一、选择题(本题有15小题,1-10题每小题3分,11-15题每小题2分,共40分。请选出各题中一个符合题意的选项,不选、多选、错选均不给分)
-
A . 豆腐发酵制臭豆腐
B . 黄豆酿酱油
C . 粮食酿酒
D . 水果榨果汁
-
2.
(2023九上·衢江月考)
土壤的酸碱度直接影响农作物的生长。已知某地区土壤显弱碱性,参照下表,从土壤酸碱性角度考虑,该地区适宜种植的作物是( )
作物 | 小麦 | 油菜 | 西瓜 | 甘草 |
最适宜的土壤pH范围 | 5.5~6.5 | 5.8~6.7 | 6.0~7.0 | 7.2~8.5 |
A . 小麦
B . 油菜
C . 甘草
D . 西瓜
-
A . 氢氧化钠、烧碱、NaOH
B . 碳酸钠、小苏打、Na2CO3
C . 碳酸钙、熟石灰、CaCO3
D . 氧化钙、消石灰、CaO
-
4.
(2023九上·衢江月考)
乌牛茶味醇气香,是茶中珍品。为了使茶树正常生长,茶农需要施加化肥(NH
4)
3PO
4 . 这种化肥属于( )
A . 氮肥
B . 钾肥
C . 复合肥
D . 磷肥
-
5.
(2023九上·衢江月考)
如图“五环旗”的上面3个环代表一种液体,下面2个环各代表一种酸碱指示剂,两环相交部分表示指示剂跟有关液体混合后显示的颜色。下列表示相交部分显示的颜色,其中显示颜色不正确的是( )

A . 红色
B . 蓝色
C . 红色
D . 蓝色
-
A . CsOH溶液能使紫色的石蕊变成红色
B . CsOH在水中的电离方程式为: CsOH=Cs2++2OH-
C . CsOH溶液能使无色的酚酞试液变红色
D . CsOH与硫酸反应生成的盐的化学式为CsSO4
-
A . 取固体药品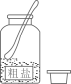 B . 稀释浓硫酸
B . 稀释浓硫酸 C . 测定溶液pH
C . 测定溶液pH  D . 向酒精灯中加酒精
D . 向酒精灯中加酒精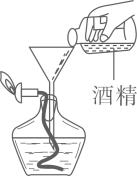
-
A . 氢氧化钠固体
B . 浓硫酸
C . 浓盐酸
D . 氢氧化铜
-
A . 2H2+O2=2H2O
B . 2HgO=2Hg+O2↑
C . Mg+2HCl=MgCl2+H2↑
D . NaCl+AgNO3=AgCl↓+NaNO3
-
A . 反应结束时溶液的pH=7
B . 氢氧化钠溶液中存在的粒子是Na+和OH-
C . 反应前后元素的种类没有变化
D . 该反应的实质是H+和OH-结合生成H2O
-
A . 固体:硝酸铵;液体:水
B . 固体:生石灰;液体:水
C . 固体:碳酸钠;液体:稀盐酸
D . 固体:氯化钠;液体:水
-
12.
(2023九上·衢江月考)
稀盐酸滴入镁粉中即产生气体,现向一定质量的稀盐酸中加入镁粉至过量,若图像中横坐标表示镁粉的质量,则纵坐标表示( )

A . 溶液的质量
B . 稀盐酸的质量
C . 氯化镁的质量
D . 生成气体的质量
-
13.
(2023九上·衢江月考)
某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是( )

A . 图中a点所示溶液呈酸性
B . 该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
C . b点表示盐酸与氢氧化钠恰好完全反应
D . 图中b点所示溶液中所含的溶质有NaCl和NaOH
-
A . Mg Fe Zn
B . CO2 SO2 CO
C . CaCO3 NaHCO3 Na2CO3
D . KOH Ca(OH)2 NaOH
-
15.
(2023九上·衢江月考)
为测定一瓶NaOH溶液是否完全变质,分别取该溶液于A、B两个密闭器中,将一定浓度的稀盐酸滴加到A中,利用二氧化碳传感器测定二氧化碳浓度变化情况,结果如图1所示;将一定浓度的氯化钙溶液(呈中性)滴加到B中,利用pH传感器测定溶液pH变化情况,结果如图2所示。下列实验结论不正确( )

A . 说明NaOH溶液是部分变质
B . 图1中ab段主要发生中和反应
C . 图2随着氯化钙溶液不断加入,pH不可能等于7
D . 根据图2,反应结束时,溶质只有NaCl
二、填空题(本题有6小题20空,每空2分,共40分)
-
-
17.
(2023九上·衢江月考)
归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示;连线表示相互反应)。

-
(1)
为了验证性质①,小红将紫色石蕊试液滴加到盐酸溶液中,溶液变色。
-
(2)
盐酸的性质③决定了盐酸可用于清除铁锈( 主要成分为Fe2O3) ,该反应的化学方程式是
-
(3)
为了验证性质⑤,可选用的物质是(填一种即可)。
-
(4)
镁和锌可以用来验证硫酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是____(填序号)。
A . 两种金属的形状
B . 盐酸的质量分数
C . 反应容器的大小
D . 温度
-
-
(1)
氢氧化钠和氢氧化钙具有相似的化学性质,原因是它们在电离时都产生了,(填微粒符号)都能使酚酞变色。
-
(2)
氢氧化钠和氢氧化钙溶液都是无色透明的液体。请选用下列任意一种物质鉴别它们,并写出相应的化学方程式
A.CO2 B.Na2CO3 C.无色酚酞
-
19.
(2023九上·衢江月考)
分析下列化学方程式表示的反应,回答有关问题:
①NaOH+NH4Cl =NaCl+NH3↑+H2O
②2KOH+ (NH4)2SO4=K2SO4+2NH3↑+2H2O
③Ca (OH)2+2NH4NO3=Ca (NO3)2+2NH3 ↑+2H2O
-
(1)
上述反应中NH4Cl、(NH4)2SO4、NH4NO3属于化肥中的 肥。
-
(2)
由上述反应可知,碱与铵盐反应的规律是都生成和水。
-
(3)
熟石灰改良过的土壤不能使用铵盐作肥料的原因是
-
20.
(2023九上·衢江月考)
用传感器探究氢氧化钠溶液与稀盐酸发生酸碱中和过程中温度和pH的变化,实验测定结果如图甲、乙所示。请回答:

-
(1)
图甲表明酸和碱的反应是反应(填“吸热”或“放热")。
-
(2)
图乙表明实验时将(填“HCl”滴入NaOH" 或“NaOH滴入HCl") 中。
-
(3)
在反应60s时的溶液中滴加酚酞试液,可观察到实验现象是
-
21.
(2023九上·衢江月考)
在道路除雪过程中,融雪剂发挥了很大的作用。某公司生产的融雪剂是由氯化钠、硝酸钾、氯化镁、硫酸铜中的二种或二种以上的物质组成的。小科为探究其成分,设计了以下实验:

请你根据以上设计过程填空;
-
(1)
该融雪剂中可能含有,肯定没有。(填化学式)
-
三、实验探究题(本题有5小老15轮。22-23题每空3分,24-26题每空2分,其36分)
-
22.
(2023九上·衢江月考)
某兴趣小组同学为探究CO
2和NaOH是否发生了化学反应,设计了如图所示的A、B实验,验证CO
2与NaOH溶液发生了化学反应。实验现象为: A中试管内液面上升,B中气球胀大。

-
-
-
(3)
李莉提出质疑,她认为上述实验不严谨,为了使实验结果更准确,更具有说服力,她设计了一个A组的对照实验C组,在水槽中加入 ,其他步骤相同。再观察比较,A组和C组试管中液面上升的高度。
-
-
-
(2)
图2中能说明氢氧化钠溶液与稀盐酸发生反应的实验现象是
-
(3)
图2反应中,下列物质能证明滴加的稀盐酸过量的是
(填序号)
A.CuO
B.AgNO3
C.CaCl2
D.pH试纸
E.Na2CO3
-
24.
(2023九上·鄞州月考)
化学兴趣小组的同学在帮助老师整理实验室时,意外地发现实验桌上有一瓶敞口放置的氢氧化钙粉末,于是对该粉末进行了如下探究.
[提出问题]该瓶粉末的成分是什么?
-
(1)
[猜想与假设]猜想一:该瓶粉末的成分可能为氢氧化钙
猜想二:该瓶粉末的成分可能为氢氧化钙和碳酸钙
猜想三:该瓶粉末的成分可能为
-
(2)
[实验验证]请你参与探究,完成下面的实验报告.
实验步骤 | 实验现象 | 实验结论 | 猜想二正确 |
①取少量样品于小烧杯中,加入适量水,充分搅拌,过滤,取少量滤渣于试管中,加入适量 | 有大量气泡发生 | 说明含有碳酸钙 |
②取步骤①中的滤液于试管中,滴加无色酚酞溶液 |
| 说明含有氢氧化钙 |
[联想与启示]氢氧化钙露置在空气中会发生变质。因此,必须密封保存.
-
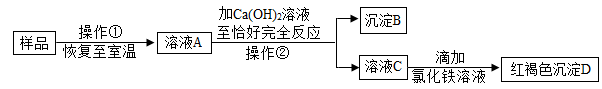
25.
实验室有一瓶敞口放置的氢氧化钠固体样品,为探究样品中的成分,小科进行如下实验:
-
-
-
(3)
小科根据实验现象认为样品中一定含有氢氧化钠,请你评价小科的判断是否正确,并说明理由。。
-
26.
(2023九上·衢江月考)
小科发现暖水瓶中有一层淡黄色的水垢。据悉,该地区的水垢中除了碳酸钙外,无其它盐类.他想探究还有没有其它物质,于是他收集水垢后经低温烘干进行下列实验:

-
(1)
取2.5g水垢按图甲中的A装置高温加热充分反应(已知CaCO
3 
CaO +CO
2),产生的气体依次通过B、C装置,实验后发现C装置中氢氧化钠溶液增加了0.88g.
①写出C装置中发现的化学反应方程式
②B装置中的浓硫酸是用来吸收反应中产生的水蒸气,这是利用了浓硫酸的性.
-
(2)
按图乙所示的方法来实验,结果发现澄清石灰水没有变浑浊,原因是
四、解答题(本题有5小题,27题4分,28题7分,29题6分,30题10分,31题7分。32题10分,共44分)
-
27.
(2023九上·衢江月考)
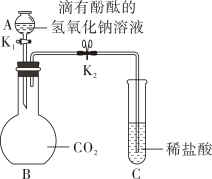
如图,关闭阀门K
2 , 缓缓打开K
1;氢氧化钠溶液进入烧瓶,轻轻震荡,发现溶液仍显红色;然后,关闭K
1 , 缓缓打开K
2 , 发现C中液体沿导管慢流入烧瓶瓶中,开始时瓶中无明显变化,后有气泡产生,且溶液红色逐渐褪去。请解释产生上述现象的原因。
-
-
(1)
尿素属于____(填标号)。
A . 氮肥
B . 磷肥
C . 钾肥
D . 复合肥
-
(2)
尿素中氮元素的质量分数是%(结果保留到小数点后一位)。
-
(3)
工业上生产尿素的反应为 :CO2+2NH3=CO(NH2)2+H2O 。若生产120t尿素,理论上需要氨气的质量是多少?(写出计算过程。)
-
29.
(2023九上·衢江月考)
石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中的碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200克,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(克) | 5 | 10 | 15 | 20 |
生成CO2的质量(克) | 1.76 | 3.52 | m | 4.4 |
-
-
-
30.
(2023九上·衢江月考)
铁放置久了会生锈(铁锈: Fe
2O
3)。小明在放置很久的铁钉中加入溶质质量分数为14.6%稀盐酸,产生氢气质量和所加稀盐酸质量关系如图所示。

-
(1)
当盐酸质量小于10g时,铁钉表面看不到明显的气泡,原因是
-
(2)
请写出加入盐酸质量0-10g时相关的化学方程式
-
-
-
31.
(2023九上·衢江月考)
食用碱的主要成分是Na
2CO
3 , (常含有少量的NaCl)。课外探究小组为测定市售某品牌食用碱中Na
2CO
3的含量,设计以下实验:取食用碱20g,逐滴滴入稀盐酸,得到数据如图所示,请根据有关信息回答问题:

-
-
-
(3)
求该盐酸中溶质的质量分数。(写出计算过程)
-
-
(1)
生物的呼吸作用、煤和石油等物质的燃烧会产生大量二氧化碳气体正常情况下,大气中二氧化碳的含量能保持相对稳定(如图),主要是因为植物的作用能吸收大量的二氧化碳气体。
-
(2)
下图表示吸收工业尾气中二氧化碳气体的一种传统方法

①生成的X固体是
②反应器中,氢氧化钠溶液喷成雾状可以使反应更充分。在科学中有很多“通过增大表面积以提高物质反应或交换效率”的例子,如人体的肺部有数量众多的肺泡可以提高气体交换效率,请你再举一个类似的例子。
-
(3)
目前,科学家正在研究“液态阳光技术”,以甲醇作为新型燃料来代替传统的煤、石油和天然气,其原理如下图所示。通过该技术,将太阳能转化为
能贮存在甲醇中。请你说出“液态阳光技术”的一个优点。


 B . 稀释浓硫酸
B . 稀释浓硫酸 C . 测定溶液pH
C . 测定溶液pH  D . 向酒精灯中加酒精
D . 向酒精灯中加酒精


















