
 B . 液晶彩电
B . 液晶彩电 C . 电烤箱
C . 电烤箱 D . 电热水壶
D . 电热水壶
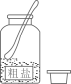 B . 稀释浓硫酸
B . 稀释浓硫酸 C . 测定溶液pH
C . 测定溶液pH  D . 向酒精灯中加酒精
D . 向酒精灯中加酒精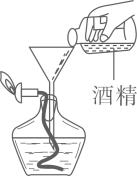
选项 | 实验目的 | 实验方案 |
A | 除去CO2中的少量氯化氢气体 | 将气体通过足量的硝酸银溶液 |
B | 除去氢氧化钠中的少量碳酸钠 | 加入过量的石灰水,充分反应后过滤 |
C | 除去锌粉中含有少量的氧化锌 | 加入足量的稀硫酸充分反应后过滤 |
D | 除去硫酸铜溶液中的少量硫酸 | 加入过量的铁粉,充分反应后过滤 |
 B .
B .  C .
C .  D .
D . 

 B . 研究氢气还原氧化铜
B . 研究氢气还原氧化铜 C . 研究影响动能大小的因素
C . 研究影响动能大小的因素 D . 研究影响唾液淀粉酶催化作用的因素
D . 研究影响唾液淀粉酶催化作用的因素



 B .
B .  C .
C .  D .
D . 


①左心室 ②肺静脉 ③主动脉 ④左心房 ⑤下肢动脉






试管编号 | 淀粉糊 | 加入的液体 | 温度 | 时间 | 加碘液 | 现象 |
1 | 2mL | 唾液2mL | 37℃ | 10min | 2滴 | ① |
2 | 2mL | 清水2mL | 37℃ | 10min | 2滴 | ② |
3 | 2mL | 唾液2mL | 5℃ | 10min | 2滴 | ③ |
4 | 2mL | 胰液2mL | 37℃ | 10min | 2滴 | 不变蓝 |


实验中观察到,甲、乙实验均有明显的实验现象。
你认为通过上述实验(填“能”或“不能”)判断出三种金属的活动性强弱。
|
上述实验后,同学们想进行废液的处理与回收,于是将甲、乙中的溶液倒入同一烧杯中,观察到混合溶液(即废液)澄清透明。同学们认为应该先确定废液中是否含有未反应完的CuSO4和AgNO3 , 为此,他们进行了实验并记录如表:
序号 | 实验操作 | 实验现象 | 实验结论 |
实验1 | 取少量废液于试管中,加入Ba(NO3)2溶液 | 产生白色沉淀 | 废液中含有未反应 完的CuSO4 |
实验2 | 取少量废液于试管中,加入A溶液 | 无明显现象 | 废液中没有AgNO3 |
讨论后大家一致认为实验1所得结论不合理。其理由应该是。
同学们尝试从废液中回收铜,于是将甲、乙中的溶液倒入同一烧杯中,再加入过量铝粉,充分反应后过滤,滤液中存在的金属阳离子是。

实验次数 | 金属球高度h/cm | 小桌腿进入细沙的深度h/cm |
1 | 20 | 1.9 |
2 | 30 | 2.9 |
3 | 40 | 3.8 |
①释放金属球时,应使金属球由“静止”开始下落。其目的是。
②根据表中数据,可以得出的结论是:。

小科同学为了探究反应所得红色固体的成分,进行了如下实验:
| 实验操作 | 实验现象 | 实验结论 |
步骤一 | 取20g红色固体于烧杯中,加入足量稀硫酸 | 红色固体可能是氧化亚铜,也可能是铜和氧化亚铜 | |
步骤二 | 将步骤一反应所得的混合物经过滤、洗涤、干燥并称量剩余红色固体质量 | 剩余红色固体质量为12g | 20g红色固体中,铜和氧化亚铜的质量比为 |


①材料:外盒是采用具有良好耐热性、保温性能的聚丙烯材料制成,餐盒为航空铝箔材料,无污染可再生。带有小孔的盒盖内扣设计,具有良好的密闭功能;
②栅格设计:内外盒之间采用栅格设计,有利于空气流动;
③发热包内含有铁粉、铝粉、焦炭粉、生石灰等物质,其中的金属粉末与碳粉在热水中能发生氧化并缓慢放热。

国家标准规定工业品纯碱指标等级 | ||||
指标项目 | 指标 | |||
Ⅰ类 | Ⅱ类 | |||
优等品 | 优等品 | 一等品 | 合格品 | |
总碱量(Na2CO3计)%≥ | 99.4 | 99.2 | 98.8 | 98.0 |
科学实践小组的同学通过实验来测定某产品的纯碱达到哪个指标等级,设计实验如图。


分别为。


结构①颜色较深,腔壁较薄,其是。(填结构名称)
脉的管壁,观察到心脏内部多处体现“结构和功能相统一”的观念。
请按照表中示例,再列举2例。
结构 | 功能 | |
示例 | 房室瓣朝心室开 | 可以防止心室的血液倒流回心房 |
① | ||
② |