选项 | 实验目的 | 实验操作 |
A | 鉴别NaCl溶液和Na2CO3溶液 | 取样,分别滴加CaCl2溶液 |
B | 检验稀盐酸中是否含有硫酸 | 取样,滴加少量Ba(OH)2溶液 |
C | 除去氯化钠中的碳酸钠 | 加入适量盐酸溶液 |
D | 分离CaCO3和CaO的混合物 | 加适量水,充分溶解后过滤 |

序号 | 实验目的 | 实验方案 |
① | 证明变质 | 取少量固体,加水溶解,滴加紫色石蕊试液。若变蓝,则说明固体未变质 |
② | 确定成分 | 取少量固体,加入足量氯化钙溶液,过滤,向滤液中滴加酚酞试液。若变红,则说明固体部分变质 |
③ | 测定纯度 | 称取ag样品与足量氯化钡溶液充分反应,将沉淀过滤,洗涤、干燥后,得到bg固体 |
④ | 除去杂质 | 取固体,加水溶解,滴加氯化钙溶液至恰好完全反应,过滤 |



其中属于氧化物的是。

I.常温下,空气中的氮气和稀有气体不会与镁发生反应。
II.无水CaCl2固体有较强的吸水性,能吸收空气中的水蒸气。
为探究镁表面黑色物质的成因是与空气中的哪些成分有关,他开展如图实验进行探究。
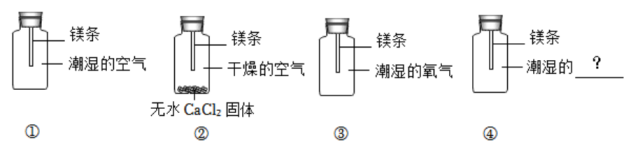
数日后第①组镁条表面出现黑色物质,第②、③组只观察到镁条表面变暗,并没有出现黑色物质。

【猜想假设】
猜想一:只含有KOH;
猜想二:含有KOH、;
猜想三:KOH、Ca(OH)2
【设计实验】
实验步骤 | 实验现象 | 实验结论 |
1.取溶液少许于试管中,滴加过量稀盐酸 | 无明显现象 | 猜想二不正确 |
2.取溶液少许于试管中,滴加少许K2CO3溶液 | 猜想三正确 |
【交流反思】
含有KOH、Ca(OH)2的废水直接排放会造成水体污染。小组同学对废水做如图处理。
C烧杯中出现现象时,说明水中已无KOH、Ca(OH)2。
①滴入酚酞溶液无明显现象②测得试管中溶液的pH小于7
③滴入BaCl2溶液有白色沉淀出现④滴入CuCl2溶液无蓝色沉淀出现

实验步骤 | 实验现象 |
步骤1:将试管A中物质全部倒入试管E中 | 产生气泡且白色沉淀增加 |
步骤2:过滤,得到滤液 | / |
步骤3:向滤液中逐滴滴加氢氧化钠溶液 | 开始无明显现象,一段时间后出现白色沉淀 |
①步骤2得到的滤液中,一定含有的溶质是(填化学式)。
②步骤3中,产生的白色沉淀是(填化学式)。
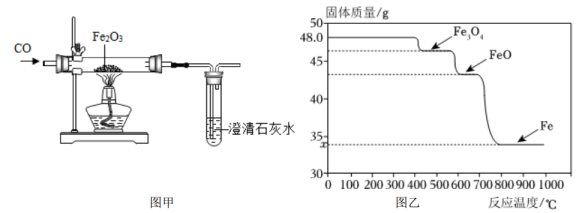
大家对乙同学提出的质疑进行分析和验证。
①用CO炼铁时,还原Fe2O3的温度应不低于℃。(填“400”“600”或“800”)
②该小组查阅资料得知酒精灯加热温度为600℃左右,他们发现上述对黑色固体成分的检验结果与图像有矛盾,推测黑色固体在冷却过程中发生了以下反应:=Fe3O4+Fe。
③在适合的条件下,Fe2O3全部被还原成Fe,则图中:x=。
 后周铁狮子
B .
后周铁狮子
B .  铸铁井盖
C .
铸铁井盖
C .  不锈钢蒸锅
D .
不锈钢蒸锅
D .  铝导线
铝导线
已知:氯化氢(HCl)是极易溶于水的无色气体,其水溶液俗称盐酸。


求:

Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1;
Ⅱ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示。
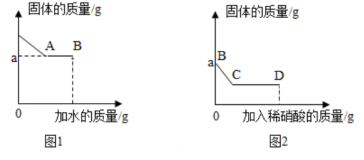
请回答下列问题:
从C到D的过程中,液体的pH将逐渐(填“增大”、“减小”或“不变”);
到达D点时,溶液中含有的溶质有种(填“—”、“二”或“三”)。
第一组 | 第二组 | 第三组 | |
反应前加入铁粉质量/g | 5.6 | 8.4 | 11.2 |
反应后剩余固体的质量/g | 3.2 | 3.2 | 6.0 |
反应后产生氢气(H2)的质量 | 0.1 | 0.2 | 0.2 |
请回答: