选项 | 实验方案 | 探究目的 |
A | 向盛有2mL | 探究 |
B | 向盛有2mL | 比较 |
C | 用注射器收集一定体积 | 探究压强对化学平衡的影响 |
D | 在一支试管中加入2mL | 探究Mg与盐酸反应的热效应 |
实验1:测得溶液的
约为
。
实验2:向酸性溶液中滴加过量
溶液,溶液紫红色褪去。
实验3:向溶液中加入等体积等浓度
溶液,溶液变浑浊。
实验4:向溶液中滴加少量等浓度
溶液,无明显现象。
若忽略溶液混合时的体积变化,下列说法正确的是( )
Ⅰ:
Ⅱ:
将一定比例的、
和
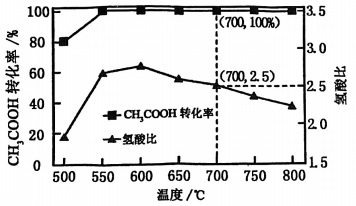
的混合气体。以一定流速通过装有催化剂的反应管,若仅考虑上述反应,
转化率、氢酸比[
]与温度的关系如题图所示。下列说法正确的是( )
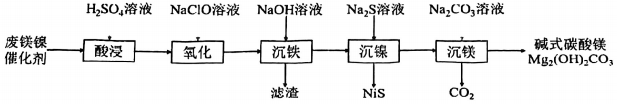
已知:25℃时,溶液中相关金属离子生成氢氧化物沉淀的pH见下表。
| ||||
开始沉淀 | ||||
完全沉淀 |
A.将废催化剂粉碎 B.适当提高搅拌速率 C.适当缩短酸浸时间
①判断达到滴定终点的标志为。
②通过上述数据,计算样品中的质量分数。(写出计算过程)
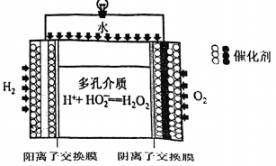
①已知分解放出
的热,在含少量
的溶液中,
的分解机理为:
Ⅰ.(慢),Ⅱ.
(快)。
下列说法正确的是____(填字母)。
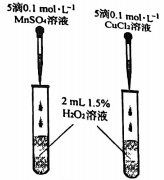
图1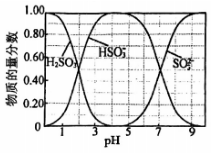 图2
图2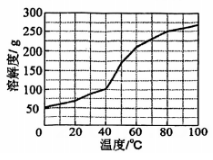
请补充完整实验方案:边搅拌边向饱和溶液中加入,停止滴加后在加热条件下,边搅拌边向其中加入硫粉至不再溶解,过滤,,用无水乙醇洗涤晶体2~3次,低温干燥。(须使用试剂:NaOH溶液)
①已知:燃烧热
;
燃烧热
;
燃烧热
。
则反应Ⅰ:。
②在基催化剂作用下,该反应的可能机理如图所示。已知
转化的表达式为
, 写出
转化为
的表达式:。
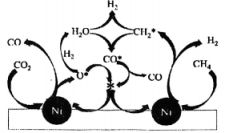
③与
重整反应制备合成气中的主要副反应为:
Ⅱ.
Ⅲ.
Ⅳ.
在、进气流速相同、
时,
做催化剂,反应相同时间测得
与
的转化率随温度变化如图所示(仅考虑上述反应)。
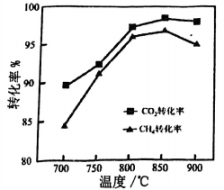
不同温度下转化率始终大于
转化率的主要原因为。
, 随温度升高
与
转化率均下降的可能原因为。
反应原理为;
。与该方法相比,
和
重整的优点是。
在密闭容器中,、
时,
与
的平衡转化率、
与
的平衡产率随温度变化如图所示。

在时,
平衡转化率为负值的可能原因为(用化学方程式表示)、。