 B . 读取液体体积
B . 读取液体体积 C . 加热液体
C . 加热液体 D . 塞紧橡胶塞
D . 塞紧橡胶塞 


选项 | 实验目的 | 实验方案 |
A | 除去氯化钾中混有的少量氯酸钾 | 加入二氧化锰加热 |
B | 除去CO2中含有的少量CO | 点燃 |
C | 鉴别H2和CH4 | 点燃,在火焰上方罩一个内壁涂有澄清石灰水的烧杯 |
D | 鉴别氮气和二氧化碳 | 将燃着的木条伸入集气瓶中 |

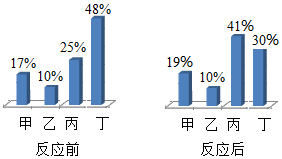
①1体积的氧气与2体积的氢气充分混合后总体积等于混合前体积之和,符合质量守恒定律;
②可燃物燃烧,必须同时满足“与氧气接触,温度达到着火点”两个条件;
③质子数相同的粒子一定是同种元素;
④某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量稀盐酸反应产生2g氢气,则该金属粉末的组成有4种情况。
①可用于制造人造骨的是。
②可用来制造铅笔芯的是。
③可用于人工降雨的是。
①2022年2月第24届北京冬奥会和冬残奥会在北京成功举办。目前世界上使用的主要能源是煤、石油和等化石燃料,对环境会产生较大的影响,为兑现我国2030年前碳达峰,2060年前碳中和的承诺,北京奥运倡导“绿色”理念。冬奥会和冬残奥会的主火炬采用无污染的氢气作为燃料,39个场馆实现了奥运史上首次100%绿色电能供应,请列举一种绿色能源。
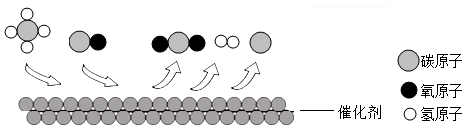
②煤的气化和液化可实现能源清洁化,改善空气质量。水煤气中CO和H,在高温、高压和催
化剂条件下合成甲醇(CH4O),下图表示该反应的原理。

参加反应的CO和H2的分子个数比为。由图可知,化学反应的微观实质是。
①3个铝原子。
②氮气。
③3个二氧化氮分子。
④硝酸根离子。

①SiO2中硅元素的化合价为价;
②反应Ⅰ的基本反应类型为反应;
③反应Ⅲ的产物有两种,其化学方程式为。

 B . 铜导线
B . 铜导线 C . 铁炒锅
C . 铁炒锅
①Fe、CuSO4溶液、Ag; ②FeSO4溶液、Cu、Ag;
③FeSO4溶液、Cu、AgNO3溶液; ④FeSO4溶液、CuSO4溶液、Ag


A.密度大于空气 B.能与水反应 C.能使澄清石灰水变浑浊
【提出问题】氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
【查阅资料】①氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
②氯气(Cl2)是有刺激性气味的气体,密度比空气大,能溶于水,能使湿润淀粉碘化钾试纸变蓝。
猜想二:该气体为;
猜想三:该气体为O2和Cl2的混合物。
序号 | 实验操作 | 实验现象 | 实验结论 |
方案1 | 用排水集气法收集甲、乙两瓶气体,将带火星的木条伸入甲瓶,湿润的淀粉碘化钾试纸伸入乙瓶。 | 木条复燃,淀粉碘化钾试纸不变色 | 猜想成立 |
方案2 | 用向上排空气法收集甲、乙两瓶气体,将带火星的木条伸入甲瓶,湿润的淀粉碘化钾试纸伸入乙瓶。 | 木条,淀粉碘化钾试纸为色 | 猜想三成立 |
①同学甲认为方案1结论不正确,其操作不合理,理由是。
②同学乙认为不需要进行实验,就能排除猜想一,理由是。
【温馨提示:NaHCO3+HCl=NaCl+H2O+CO2↑】
请分析并计算:
