|
|
|
|
A.氢氧化铝用于治疗胃酸过多 | B.铁质水龙头上镀铬延长使用寿命 | C.氢氧化钠用于生产肥皂 | D.用炉具清洁剂 清洗餐具 |
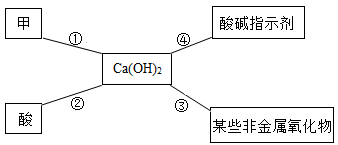
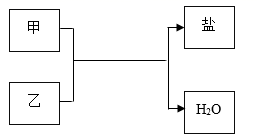
| 选项 | 甲 | 乙 |
| A | Fe2O3 | 稀硫酸 |
| B | SO3 | NaOH溶液 |
| C | 稀盐酸 | Ca(OH)2溶液 |
| D | 稀盐酸 | AgNO3溶液 |


 B .
B .  C .
C .  D .
D . 
①当图2中两种溶液恰好完全反应时,对应的是图3中的点(填“A”“B”或“C”),图4中的点(填“a”“b”或“c”)。
②图4中的c点溶液呈性,此时溶液中含有的阳离子是填离子符号)。
总结一:硫酸的化学性质

①写出氧化铁与硫酸的化学方程式.
②补充一个实验,完善硫酸的化学性质,X可以是(用化学式表示).
③能发生中和反应的化学方程式.
④为测定某硫酸中溶质的质量分数,甲同学取该硫酸样品50g,向其中加入过量锌粒,充分反应后收集到0.2克氢气,请完成下列计算与分析:
Ⅰ.收集到的氢气是: mol
Ⅱ.计算:该硫酸中溶质的质量分数.(根据化学方程式计算于上方空白处)
总结二:氢氧化钙的化学性质

(已知:CaCl2溶液呈中性,CaCl2+Na2CO3→CaCO3↓+2NaCl)
⑤乙同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈(填“酸性”、“碱性”或“中性”).
⑥丙同学将过量的稀盐酸加入到乙同学所得溶液中,观察到红色褪去,此时所得溶液中含有的溶质有(酸碱指示剂除外).请设计实验证明盐酸过量:,
⑦丁同学将碳酸钠溶液加入滴有酚酞的氢氧化钙溶液中,充分反应后,观察到的
现象:; 反应后溶液中的溶质有.

①实验甲中,观察到的现象为。
②实验乙中,反应的化学方程式为。
③实验丙中,将足量氢氧化钠溶液滴入锥形瓶后振荡,观察到的现象为。
实验结束后,同学们将甲、乙、丙三个实验的废液和废渣倒入同一个干净的废液缸中,观察到固体消失,废液呈无色。
【资料卡片】:氯化钙溶液呈中性;
【提出问题】无色废液中含有哪些溶质?
【作出猜想】
猜想一:NaCl、
猜想二:NaCl、HCl
猜想三:NaCl、HCl、
小组同学讨论后认为猜想二是不合理的,理由是。
【实验设计】小组同学对取样无色废液后,逐滴滴入碳酸钠溶液证明了猜想三是成立的。实验中应获取的证据为,发生的化学方程式为。
【反思总结】通过以上探究实验,可归纳出碱的化学性质有。


Ⅰ、向滴加有酚酞的NaOH溶液中慢慢滴入稀盐酸(如图1所示),边滴加边振荡,测得试管①中最终溶液的pH=2。
Ⅱ、分别称取0.5g氢氧化钙粉末置于两支试管中,各滴加2mL水,振荡;再向试管②中加入2mL水、试管③中加入2mL稀盐酸(如图2所示)。振荡并观察现象。
Ⅲ、向盛有氢氧化钠溶液的试管④中加入少量硫酸铜溶液,振荡。静置后测得上层清液的pH=12,继续向其中滴加几滴稀盐酸(如图3所示),试管⑤中无明显现象。
实验Ⅰ中,能证明盐酸和氢氧化钠发生了化学反应的实验现象是。试管①最终溶液中含有的溶质有(酚酞除外)。
【实验探究二】取试管①反应后的溶液逐滴滴入试管⑤中,直至过量,边加边振荡。
实验探究二中依次观察到的现象有。
【结论】盐酸能与Cu(OH)2发生反应。
【交流反思】最终试管⑤溶液中大量存在的离子有。

【提出问题】怎样证明C、D试管中发生了反应?
【分析讨论】同学们讨论后认为,可以用两种思路探究上述反应是否发生。
思路1:验证反应物减少或消失:思路Ⅱ:验证有。
实验操作 | 实验现象 | 实验结论 |
取少量D中反应一段时间后的溶液于试管中,向其中加入 | 氢氧化钠溶液与二氧化碳发生了反应 |