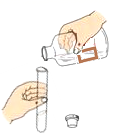
 取用液体药品
C .
取用液体药品
C . 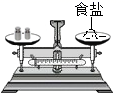 称量食盐
D .
称量食盐
D . 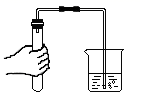 检查装气密性
检查装气密性
①分子种类;②原子种类;③分子数目;④原子数目;⑤各物质的质量总和.
选项 | 实验目的 | 实验方案 |
A | 除去混入CO2中的CO | 点燃 |
B | 除去MnO2中的CuO | 加入足量的水溶解,过滤 |
C | 除去CaO溶液中混有的CaCO3 | 加入蒸馏水中,过滤 |
D | 除去混入CO中的CO2 | 通入澄清石灰水 |
物质 | W | G | H | P |
反应前质量/g | 18 | 1 | 2 | 32 |
反应后质量/g | 待测 | 26 | 2 | 12 |
对该反应的认识正确的是
②鉴别硬水和软水物质是;燃烧的条件是物质具有可燃性、与氧气接触、同时。
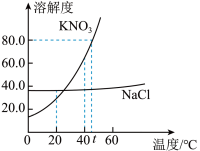
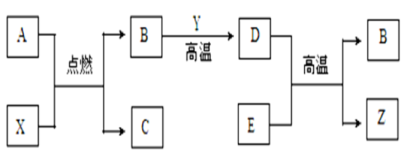
请根据以上信息回答下列问题:
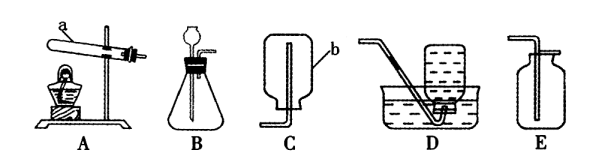
【实验目的】 探究二氧化锰是氯酸钾受热分解的催化剂。
【药 品】 二氧化锰、氯酸钾
【仪 器】 木条、火柴、试管夹、试管、药匙等仪器。
【实验内容】
实验操作 | 实验现象 | 实验结论或总结 | |
1.将氯酸钾加热至融化,用带火星的木条检验氧气。 | 加热较长时间,木条复燃。 | 氯酸钾受热分解产生氧气。 | 总 结 二氧化锰是氯酸钾受热分解的催化剂 |
2.加热二氧化锰,用带火星的木条检验氧气。 | 木条 | 二氧化锰受热不产生氧气。 | |
3.将MnO2与KClO3的混合物加热,用带火星的木条检验氧气。 | 木条迅速复燃。 | 二氧化锰能 氯酸钾的分解速度。 | |
根据催化剂的特点,上述探究实验还不能完全得出表内“总结”,还需设计一些实验,验证二氧化锰是氯酸钾受热分解的催化剂。要证明MnO2(不溶于水)在KClO3分解前后不变,待氯酸钾完全受热分解后,把反应后的物质通过、、洗涤、烘干等操作才能得到纯净、干燥的二氧化锰,……。