| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
固体的质量/g | 30 | 60 | 30 | 60 | 90 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
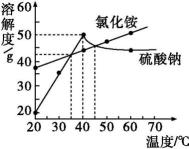
下列关于①~⑤所得溶液的说法不正确的是( )
溶液 | 碳酸钠溶液 | 高锰酸钾溶液 | 碘酒 | 食盐水 |
溶质 | KMnO4 | |||
溶剂 | H2O |

编号 | 溶剂 | 溶质 | 现象 |
A | 水 | 碘 | 试管底部有固体,液体呈淡黄色 |
B | 汽油 | 碘 | 试管底部无固体,液体呈紫红色 |
①实验目的是。
②将试管B中的液体密封放置一段时间后,不会出现浑浊现象,为什么?。
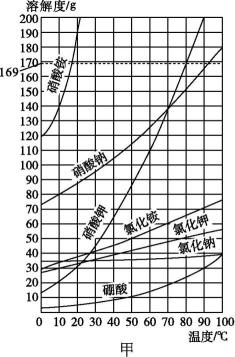
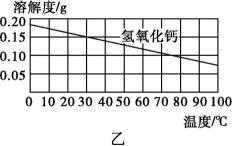
①根据图甲、图乙分析,固体物质的溶解度随温度的变化有什么规律,完成填空:少数固体物质的,如氯化钠;极少数固体物质的,如氢氧化钙。
②80 ℃时,将200 g KNO3固体放入100 g水中,充分溶解后,所得溶液的质量为g。
③KNO3中混有少量的NaCl,可用的方法提纯KNO3。
温度/ ℃ | 0 | 10 | 20 | 30 | 40 | 50 |
溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
温度/ ℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解 度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |

①操作1的名称是。x=g,固体c的成分是。
②对整个实验过程分析正确的是(填字母)。
A.40~60 ℃开始析出晶体
B.氯化钠在整个过程中一直保持不饱和状态
C.上述方法不能将氯化钠和硝酸钾完全分离
D.原溶液直接冷却热饱和溶液,析出硝酸钾的质量不变
探究一:溶解过程中的能量变化
如图所示,同学们设计了不同的实验方案进行探究:
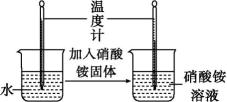
实验一 硝酸铵的溶解

实验二 氢氧化钠的溶解
如图是配制50 g溶质质量分数为10%的氯化钠溶液的有关操作示
意图:
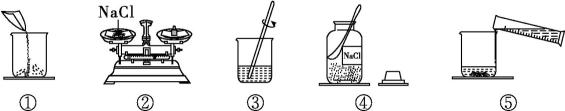
需要称取氯化钠的质量是g,称量时出现了指针偏向右盘的现象,接下来的操作是。
“100 mL”)的量筒,读数时视线应该与保持水平。
