一、选择题(本题含20小题,每小题2分,共40分。每小题只有一个符合题意的选项。)
-
1.
(2024·梧州模拟)
2024年世界环境日中国的主题为“全面推进美丽中国建设”。下列与该主题不符合的做法是( )
A . 大力开发利用水力发电
B . 直接排放工业废气
C . 分类回收处理生活垃圾
D . 减少使用一次性制品
-
A . 氧气具有可燃性
B . 氧气的质量分数约为21%
C . 稀有气体可用于制造电光源
D . CO2、SO2属于空气污染物
-
A . 氢能
B . 太阳能
C . 化石能源
D . 风能
-
4.
(2024·梧州模拟)
下列实验基本操作中,正确的是( )
 | 
|
A.滴加液体 | B.倾倒液体 |

| 
|
C.取用固体 | D.量取液体 |
A . A
B . B
C . C
D . D
-
A . 食盐
B . 蔗糖
C . 白醋
D . 面粉
-
A . O
B . Ca
C . Na
D . N
-
A . Zn
B . Al
C . Mg
D . Ag
-
A . 雾霾专用口罩中有活性炭,它能吸附有害气体
B . 温度计内汞柱液面上升,说明汞原子的间隔变大
C . 甲醛溶液有防腐作用,可用来保鲜食品
D . 氢气和液氢都可作燃料,说明同种分子的化学性质相同
-
-
A . NaOH
B . Na2CO3
C . H2CO3
D . CaO
-
A . 镁是一种非金属元素
B . Mg2+得到电子可变成Mg
C . 镁离子核外有三个电子层
D . 镁的相对原子质量为24.31g
-
A . 橙汁(3~4)
B . 鸡蛋清(7~8)
C . 牙膏(8~9)
D . 清洁剂(12~13)
-
A . 随意丢弃废旧金属
B . 将铁锹放置于潮湿的空气中
C . 用PVC塑料管替代铁制下水道
D . 把铁制品表面的油膜洗净以防止锈蚀
-
A . +6
B . +3
C . +2
D . 0
-
A . 试管中的细沙可以防止试管炸裂
B . 实验说明氧化钙与水反应放出热量
C . 实验结束后量筒中的水最终减少了10mL
D . 实验结束后试管内气体的主要成分为氮气
-
A . 身体着火,应就地打滚熄灭火
B . 炒菜时油锅着火,可用水浇灭
C . 高层建筑物起火,立即乘电梯撤离
D . 夜间发现煤气泄漏,立即开灯检查
-
A . CO2→CaCO3→Ca(OH)2
B . CO2→CO→Fe
C . Na2CO3→NaCl→MgCl2
D . H2SO4→BaSO4→Ba(NO3)2
-
18.
(2024·梧州模拟)
下列实验方案,不能达到实验目的的是( )
选项 | 实验目的 | 实验设计 |
A | 鉴别氯化铵和氯化钾 | 加入熟石灰固体研磨,闻气味 |
B | 检验甲烷中含氢元素 | 点燃,在火焰上方罩一个冷而干燥的小烧杯 |
C | 提纯混有少量泥沙的氯化钠 | 溶解、过滤、蒸发、结晶 |
D | 除去NaCl溶液中的Na2SO4 | 滴加适量的稀盐酸溶液,过滤 |
A . A
B . B
C . C
D . D
-
19.
(2024·梧州模拟)
下图为KNO
3、Na
2CO
3、NaCl固体(均不含结晶水)的溶解度曲线,下列判断正确的是( )

A . KNO3的溶解度大于NaCl的溶解度
B . t2℃时,将上述三物质的饱和溶液降温至t1℃,析出晶体最少的是NaCl
C . t1℃时,将上述三种物质的饱和溶液升温至t2℃,所得溶液的溶质质量分数大小关系为:KNO3=NaCl>Na2CO3
D . 当KNO3中混有少量的NaCl时,可采用蒸发结晶的方法提纯KNO3
-
20.
(2024·梧州模拟)
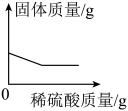
向盛有一定量氧化铁的烧杯中不断滴入稀硫酸,烧杯中有关量的变化见下图,其中正确的是( )
二、填空题(本大题共5小题,每个化学方程式2分,其余每空1分,共26分,)
-
-
22.
(2024·梧州模拟)
化学使我们的生产、生活更加美好。请用下列物质的序号填空。
①氖气②生石灰③钛合金④硫酸铜⑤小苏打
-
-
-
-
-
-
23.
(2024·梧州模拟)
梧州六堡茶文化源远流长,煮上一壶好茶,茶汤滋味醇厚、柔滑回甘,吸引不少外地旅客前来品尝。
-
(1)
净水:好茶用好水。城市生活用水是经自来水厂净化处理过的,主要步骤为河水→沉降→过滤→吸附→消毒→净化的水。
①净水过程中,在沉淀池加入明矾的作用是。
②消毒过程中,常用液氯作为消毒剂,反应的微观示意图如图所示,该反应的化学方程式为。

-
(2)
煎茶:好壶配好茶。烧制茶壶的过程中,发生的其中一个化学反应为:

, X的化学式为
,判断依据是
。
-
(3)
泡茶:古代常用锡器(Sn)来泡茶,时间长久会在锡器表面形成+4价的氧化物,该氧化物的化学式为。
-
-
-
-
(3)
铝制品有良好的抗腐蚀性,主要原因是:(用化学方程式表示)。
-
(4)
太阳能电池目前广泛使用硅基材料。晶体硅的结构与金刚石类似,也是由(填“分子”“原子”或“离子”)构成的。
-
-
(1)
实验1中,反应前后溶液中没有变化的离子是
。

-
(2)
实验2的反应现象是
。

-
(3)
实验3发生反应的化学方程式是
。

-
(4)
上述实验结束后,化学兴趣小组继续探究。
步骤 | 现象 | 分析与结论 |
将实验3试管中的物质过滤,再将滤液与另两支试管中的溶液全部混合,使其充分反应 | 产生气泡,生成白色沉淀A | 沉淀A所有可能的成分是(填化学式) |
三、简答题(本大题共2小题,每个化学方程式2分,其余每空1分,共12分。)
-
-
(1)
长征二号F运载火箭的燃料是偏二甲肼(C2H8N2),偏二甲肼中碳元素的质量分数为,偏二甲肼燃烧属于变化。
-
(2)
航天飞船会使用一种材料,这种材料是在碳化硅、陶瓷中嵌入碳纤维而制成的,它属于____材料(填字母序号)。
A . 金属材料
B . 复合材料
C . 合成材料
D . 有机材料
-
(3)
航天飞船座舱内空气更新过程的示意图如图所示。

①装置I的作用是。
②一定条件下,CO2和H2在装置Ⅱ内发生反应,该反应的化学方程式为。
-
27.
(2024·梧州模拟)
实验室可用某种石灰石(含少量Fe
2O
3杂质)为原料,模拟工业制备高纯CaCO
3 , 其流程如图所示,请回答下列问题:

-
(1)
“酸溶”前为使反应物充分接触,应对石灰石进行的操作是。
-
(2)
①“沉钙”时先通入氨气再通入二氧化碳的原因是
。
②“沉钙”时发生反应的化学方程式为:。
-
-
(4)
“沉钙”过程中,若其他条件不变,当温度高于35℃时,CaCO3的产率会明显下降,其主要原因:一是氨水挥发和分解速率加快,二是。
四、实验探究题(本大题共2小题,每个化学方程式2分,其余每空1分,共16分。)
-
-
-
(2)
实验室制取氢气可选用的发生装置和收集装置是(填字母序号)。
-
(3)
用装置B制氧气的化学方程式为,制取气体时,放入药品前应先进行的操作是。
-
(4)
用装置E收集满一瓶气体,检验此气体为氧气的方法是(请将操作、现象、结论描述出来)。
-
(5)
若用装置F收集二氧化碳,气体应从(填a或b)导管进。
-
(6)
如图G所示,向烧杯中倒入二氧化碳,观察到的实验现象为。
-
29.
(2024·梧州模拟)
“暖宝宝”是一种生活常用物品。同学们对“暖宝宝”的发热原理及成分充满好奇,在老师的指引下,他们开展了“暖宝宝的秘密探索”项目实践活动。
-
(1)
任务一:探究“暖宝宝”的发热原理
【查阅资料】
①“暖宝宝”袋内为黑色固体,主要成分有铁粉、活性炭、氯化钠、蛭石、水等,除氯化钠外,其他成分不含氯元素。
②蛭石是一种硅酸盐矿物,属于保温材料。
【实验探究】
拆开“暖宝宝”的外包装,发现“暖宝宝”的温度逐渐升高。冷却后,拆开“暖宝宝”的内包装,发现黑色粉末中掺杂有红棕色的固体。小组讨论得知“暖宝宝”的发热原理为:铁粉与空气中的共同作用发生缓慢氧化放出热量。
-
(2)
任务二:验证“暖宝宝”的主要成分
取少量未曾使用过的“暖宝宝”内的固体分别进行以下操作
实验步骤 | 实验现象 | 实验结论 |
步骤1:取少量固体于试管中,加入足量稀硫酸。 | 观察到。 | 固体中含有铁 |
步骤2:取少量固体于燃烧匙中,在酒精灯上加热,上方罩一个内壁沾有澄清石灰水的烧杯(如图8所示)。 | 澄清石灰水变浑浊 | 固体中含有活性炭 |
步骤3:取少量固体于烧杯中,加入足量水溶解,过滤,往滤液滴加少量不溶于稀硝酸。 | 产生白色沉淀,沉淀溶液和稀硝酸。 | 固体中含有氯化钠 |
-
(3)
【反思与评价】
小吴认为步骤2不能得到固体中含有活性炭的结论,理由是。
-
(4)
任务三:测定“暖宝宝”中活性炭的质量分数

为了准确检测固体中含有活性炭,并测定“暖宝宝”中活性炭的质量分数,同学们设计了如图所示的实验装置。(实验前已排尽装置内的空气,B、C、D中药品均足量,碱石灰是NaOH和CaO的固体混合物)。

装置C的作用是。
-
(5)
为了测定“暖宝宝”中活性炭的质量分数,需测定反应前“暖宝宝”固体的质量及反应前后(填装置编号)装置增重的质量。
-
(6)
小周同学提出,不需要装置E也可以达到实验目的,遭到了大多数同学的反对,理由是。
-
(7)
【拓展延伸】
“暖宝宝”中活性炭和氯化钠有何作用?同学们通过对比生活中铁生锈与“暖宝宝”发热的具体情况,作出大胆猜想,认为氯化钠与活性炭的作用为。
五、计算题(本题共6分)
-
30.
(2024·梧州模拟)
现有碳酸钠和氯化钠的固体混合物13.25g,兴趣小组为研究其成分,将13.25g样品放入烧杯中,再向其中逐滴加入127.9g稀盐酸,反应生成二氧化碳的质量与所加入的稀盐酸的质量关系如图所示。

-
-
(2)
计算该样品中氯化钠的质量分数。(写出计算过程)。



 B .
B . 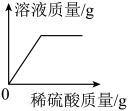 C .
C . 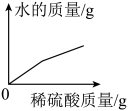 D .
D . 









