 B . 点燃酒精灯
B . 点燃酒精灯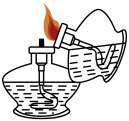 C . 加热液体
C . 加热液体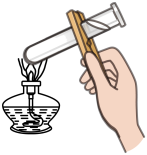 D . 稀释浓硫酸
D . 稀释浓硫酸



序号 | 物质 | 杂质 | 试剂及操作 |
A | 铁粉 | 铜粉 | 足量硫酸溶液、过滤 |
B | KNO3 | NaCl | 冷却热饱和溶液 |
C | CuCl2溶液 | FeCl2 | 过量铁粉、过滤 |
D | KCl溶液 | MgCl2 | 过量KOH溶液、过滤 |
|
|
|
|
A.向盛有NaOH溶液的烧杯中滴加稀盐酸 | B.加热氯酸钾和二氧化锰的固体混合物 | C.在一定温度下,配制氯化钾饱和溶液 | D.将足量的镁粉和锌粉分别加入到等量且质量分数相等的稀硫酸中 |


实验较长时间后,发现试管中铜片最先生锈(填试管字母编号).小区认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验.你认为要补充的一个实验是.(用文字描述或者画图)

1799年,伏特把一块锌板和一块锡板浸在盐水里,发现连接两块金属的导线中有电流通过,制成了世界上第一块电池——“伏特电堆”。1836年,英国的丹尼尔对“伏特电堆”进行了改良,削成了如图1所示的电池。电池几经变化,演变成现在的多种电池,其中用量最大是普通干电池,其结构如图2所示。普通干电池电压随使用时间而下降,直至报废,所以也称为一次性电池。给电池以反向电流,使电池电压回升。能反复使用的电池称为“蓄电池”。汽车用铅酸电池充电时发生反应的化学方程式为2PbSO4+____═PbO2+Pb+2H2SO4。燃料电池又称“连续电池”,即只要活性物质连续地注入,就能不断地进行放电的一类电池,专用于燃料电池电动汽车(如图3),氢燃料电池就是其中的一种,它靠氢气在空气中燃烧产生电能。
依据短文回答下列问题:

已知:①钛铁矿主要成分为钛酸亚铁(FeTiO3)。
②钛铁矿浸在浓硫酸中发生反应:

①将过氧化氢溶液缓慢推入装置,c处看到的现象是 ,该反应的化学方程式为 ;观察到e处白磷燃烧而d处红磷不燃烧,说明燃烧需要具备的条件是 。
②若想让e处燃着的白磷停止燃烧,可使用的方法是 。

甲 乙 丙
探究一:
图甲所示试管内没有观察到明显现象,那么该如何设计实验来探究氢氧化钠和稀硫酸是否发生反应呢?
【实验反思】同学们对反应后硫酸是否剩余继续进行验证,进行如下实验:
组号 | 操作 | 实验现象 | 结论 |
1 | 用pH试纸测定实验后溶液的pH | pH=3 | 硫酸剩余 |
2 | 向反应后的溶液中加入适量Ba(NO3)2溶液 | 产生白色沉淀 | 硫酸剩余 |
3 | 向反应后的溶液中加入适量镁条 | ? | 硫酸剩余 |
(填“偏大”“偏小”或“不变”)。
图乙所示实验中装置B内发生的化学方程式为 ,要证明NaOH与CO2发生了化学反应,兴趣小组做了图丙的数字化实验,则图3中的曲线(填“A”或“B”)表示氢氧化钠溶液与二氧化碳的反应;向二氧化碳中加入80mL蒸馏水的目的是。
实验操作 | 实验现象 | 实验结论 |
取样于试管中,先滴加足量的 溶液,过滤后,再往滤液中滴加少量 溶液。 | 开始有白色沉淀生成,加入另一种试剂溶液变红色 | 碳酸钠和氢氧化钠 |
结果表明,0.5L水样反应时产生了2.54×10﹣3mg的I2。