物质 | 牛奶 | 蔗糖水 | 鸡蛋清 | 炉具清洁剂 |
pH | 6.3~6.6 | 7 | 7.6~8.0 | 12~13 |
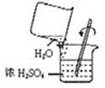 B .
B . 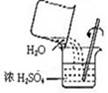 C .
C . 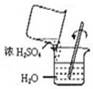 D .
D . 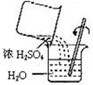
 B .
B .  C .
C .  D .
D . 
序号 | 甲 | 乙 |
① |
| KOH溶液 |
② | Ag-Zn合金 | 稀 |
③ | 久置空气中的铝片 | 稀盐酸 |
④ | 含有 | 稀 |
⑤ | HCl和 |
|

实验方案 | 使用的试剂 | 判断的方法 |
A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
B | pH试纸 | 如果pH<7,表明盐酸已经过量 |
C | 硝酸银溶液 | 如果有白色沉淀产生,表明盐酸已经过量 |
D | 紫色石蕊试剂 | 如果溶液变成红色,表明盐酸已经过量 |

①食盐是白色晶体②氨气有刺激性气味③酒精挥发④浓硫酸有腐蚀性
⑤碱石灰能吸收CO2⑥铁丝生锈⑦铜能导电⑧蔗糖在水中溶解




【提出问题】氢氧化钠固体是否变质?
【实验探究】甲、乙两同学分别设计了不同方案加以实验。
甲同学的方案及实验:
实验步骤 | 实验现象与结论 |
①取少量白色固体于试管中,加水振荡至全部溶解 | 无色溶液 |
②用pH试纸测①溶液的pH值 | 溶液的 |
乙同学的方案及实验:
实验步骤 | 实验现象与结论 |
①取少量白色固体于试管中,加水进行振荡至全部溶解 | 无色溶液 |
②向①溶液中加入适量氯化钡溶液 | 产生白色沉淀,说明氢氧化钠固体已变质 |

实验编号 | |||||||||
溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
水的温度(℃) | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 70 |
溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
请回答:

查阅资料:电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小,相同温度同种溶液导率越大,表示离子浓度越大.
①M点前曲线下滑的原因是。M点溶液中存在的微粒是。
②为验证N点对应溶液中稀盐酸有剩余,可往溶液中加入来证明。

温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
铁钉质量增加/g | 0.02 | 0.04 | 0.08 | 0.16 | 0.18 | 0.18 | 0.18 |
①该实验能得出的结论是。
②铁钉生锈主要和空气中的有关。有同学认为该实验未能真实反映50℃以后铁钉锈蚀的快慢,理由是:50℃以后铁钉质量没有变化。请分析表格中数据并结合生锈原因说明铁钉质量没有变化的原因是。


模型评价表
评价指标 | 优秀 | 合格 | 待改进 |
指标一 | 密封性好,能除去大部分污染气体 | 密封性好,能除去小部分污染气体 | 密封性不好,不能除去污染气体 |
指标二 | 能通过实验现象说明煤燃烧产生的气体是 | 有实验现象,但不能说明煤燃烧产生 | 没有明显实验现象 |
指标三 | 能通过多个实验现象显示酸雨的危害 | 能通过一个实验现象显示酸雨的危害 | 不能通过实验现象显示酸雨的危害 |


【实验数据】实验共记录了两组数据:
第①组,气体吸收完全后,NaOH溶液质量增加4.4g;
第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g。
根据实验设计及有关数据进行分析与计算:
实验组数 | 第一组 | 第二组 | 第三组 |
加入氢氧化钠溶液质量/g | 50 | 100 | 80 |
产生沉淀的质量/g | 0.98 | 2.94 | 2.94 |

请根据以上信息回答下列问题: