
 B .
B .  C .
C .  D .
D . 
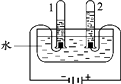
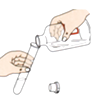 B . 加热液体
B . 加热液体 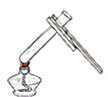 C . 点燃酒精灯
C . 点燃酒精灯 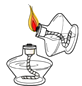 D . 检验气密性
D . 检验气密性 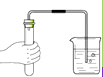
选项 | 实验目的 | 实验操作 |
A | 鉴别二氧化碳和氮气 | 将燃着的木条伸入集气瓶中 |
B | 除去CO2中的少量CO | 点燃 |
C | 检验H2中混有的CH4 | 点燃,在火焰上方罩一个干冷烧杯 |
D | 鉴别H2O2溶液和H2O | 分别加入二氧化锰 |
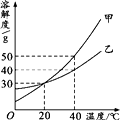
 B .
B . 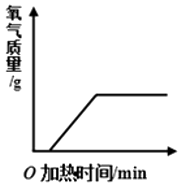 C .
C . 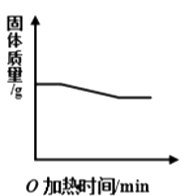 D .
D . 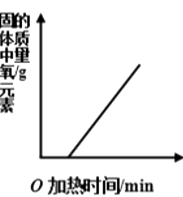
 B . 加碱反应
B . 加碱反应  C . 竹帘捞纸
C . 竹帘捞纸  D . 剪裁纸张
D . 剪裁纸张 
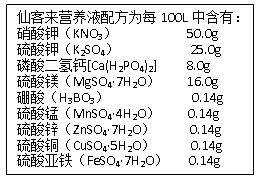
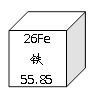
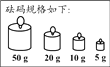
 B . 100mL量杯
B . 100mL量杯  C . 500mL量杯
C . 500mL量杯 
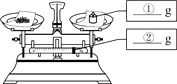
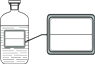
A | B |
向一盛有少量干冰的玻璃容器中加入适量热水,立即产生浓厚的白雾,产生此现象的原因是 另取一盛有适量澄清石灰水的玻璃容器,向其中加入少量干冰,观察到澄清石灰水变浑浊,发生反应的化学方程式为。 |
点燃蜡烛后,电子秤示数逐渐减小。蜡烛减小的质量(填“大于”“等于”或“小于”)燃烧后生成物的总质量。
用玻璃杯迅速扣住燃烧的蜡烛,并使杯口始终浸没在水中最终杯中液面(填“高于”“等于”或“低于”)碗中液面。 |
咸鸭蛋是人们常用的一种食品,咸鸭蛋黄还是制作粽子、点心等食品的材料。咸鸭蛋中富含锌、钙,对儿童身体及骨骼的生长有帮助,并能在一定程度上预防贫血。
资料1:腌制原理
咸鸭蛋在腌制过程中,食盐通过蛋壳及蛋壳膜不断向蛋内渗透,虽然没有改变蛋白质及脂肪的成分,但却改变了蛋白中蛋白质的特性及蛋黄中脂质含量。
资料2:腌制过程
腌制鸭蛋一般经过以下几个步骤:鲜蛋→检验(照蛋)→洗蛋→晾干→放入食盐水溶液中装罐→腌制。一般腌制30天,就能得到味美的咸鸭蛋。资料显示,将晾干后的鲜鸭蛋放入1%的盐酸溶液中浸泡10分钟,蛋壳(主要成分是CaCO3)与盐酸溶液发生反应,蛋壳表面的毛孔增大。放入饱和的食盐水中,溶液更易通过蛋膜进入蛋清,只需7天左右就可腌制出合格的咸蛋(蛋内的食盐含量及蛋黄内的油脂含量均达到国家标准),且口感很好。
资料3:影响咸鸭蛋品质的因素
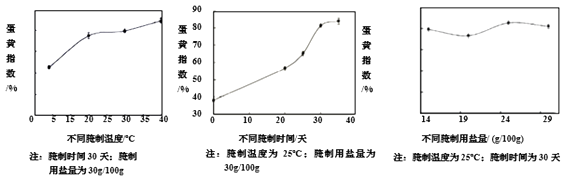
咸鸭蛋的蛋黄指数是鸭蛋品质的一个重要指标。一般情况下,蛋黄指数越高,品质越好。不同腌制条件对蛋黄指数的影响如下所示。
资料4:咸鸭蛋的食用
咸鸭蛋与鲜蛋的营养价值基本相同,但咸鸭蛋中钠、钙、铁、硒等矿物质元素含量比鲜鸭蛋高。特别是含钠量高,折算成含盐量,每只咸蛋含盐在6g以上。长期高盐摄取是造成高血压、胃粘膜受损等疾病的原因。
依据文章内容,回答下列问题。

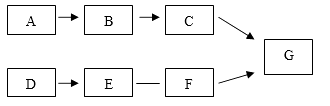


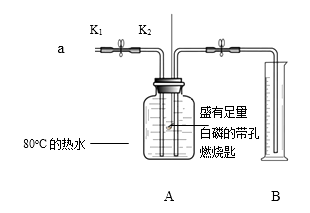
步骤I.检查装置的气密性。
步骤II.将盛有足量白磷的带孔燃烧匙伸入A瓶中,向瓶中加满80℃热水,塞紧瓶塞。
步骤III.打开K1、K2 , 从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2。此时量筒中水的体积为200mL。
![]()
【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与铜片接触的物质,利用右图装置(铜片长
8cm,宽1cm,试管容积为20mL),分别进行下列7个实验,并持续观察30天。
编号 | 主要实验操作 | 实验现象 |
① | 充满纯净的O2 | 铜片均无明显变化 |
② | 充满纯净的CO2 | |
③ | 充满经煮沸并迅速冷却的蒸馏水 | |
④ | 加入蒸馏水5mL(液面未浸没铜片),再充满O2 | |
⑤ | 加入经煮沸并迅速冷却的蒸馏水5 mL,再充满CO2 | |
⑥ | 充入10mL O2 , 再充入10mLCO2 | |
⑦ | 加入蒸馏水5mL,再依次充入10mL CO2和10mL O2 | 铜片生锈,且水面附近锈蚀最严重 |
【解释与结论】
请写出一种防止铜制品锈蚀的方法。