
 光合作用
B .
光合作用
B .  烧炭取暖
C .
烧炭取暖
C .  风力发电
D .
风力发电
D .  电解冶炼
电解冶炼
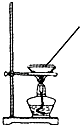 B .
B .  C .
C . 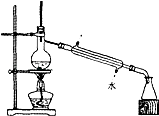 D .
D . 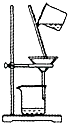

①高铁座椅内填充有聚氨酯软质泡沫.聚氨酯属于(填字母).
a.金属材料 b.无机非金属材料 c.有机高分子材料
②高铁信息传输系统中使用了光导纤维.光导纤维的主要成分是(填字母).
a.铜 b.石墨 c.二氧化硅
③高铁轨道建设需用大量水泥.生产水泥的主要原料为黏土和(填字母).
a.石灰石 b.粗盐 c.纯碱.


已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
FeS2+14Fe3++8H2O=15Fe2++2SO42﹣+16H+
离子 | 离子浓度(mol•L﹣1) | |
还原前 | 还原后 | |
Fe2+ | 0.10 | 2.5 |
SO42﹣ | 3.5 | 3.7 |
请计算反应Ⅰ、Ⅱ中被还原的Fe3+的物质的量之比(写出计算过程).