|
实验编号 |
盐酸浓度/(mol/L) |
铁的形态 |
温度/K |
|
① |
4.00 |
块状 |
293 |
|
② |
4.00 |
粉末 |
293 |
|
③ |
2.00 |
块状 |
293 |
|
④ |
2.00 |
粉末 |
313 |
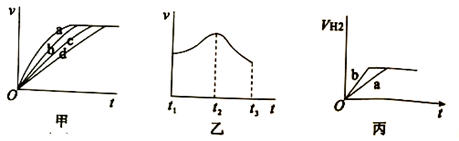
①其中t1~t2速率变化的主要原因是。
②t2~t3速率变化的主要原因是 。