① 已知上述反应中生成 1 mol NH3 放出 46 kJ 热量,该反应的热化学方程式为。
②该反应放热,但仍选择较高温度。其原因是。
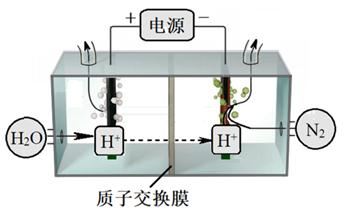
① 阴极生成氨的电极反应式为。
② 阳极氧化产物只有 O2。电解时实际生成的 NH3 的总量远远小于由 O2 理论计算所得 NH3 的量,结合电极反应式解释原因:。
![]()
已知:氮原子利用率是指目标产物中氮的总质量与生成物中氮的总质量之比
上述反应③的氮原子利用率为 66.7%。要使原料 NH3 转化为 NH4NO3 的整个转化过程
中氮原子利用率达到 100%,可采取的措施是
微信扫码预览、分享更方便