(15分)某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含 量过低,对实验的影响可忽略).
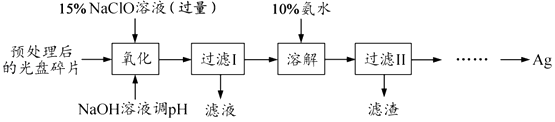
已知:①NaClO溶液在受热或酸性条件下易分解,如 3NaClO═2NaCl+NaClO3
②AgCl可溶于氨水 AgCl+2NH3•H2O⇌Ag(NH3)2++Cl﹣+2H2O
③常温时 N2H4•H2O(水合肼)在碱性条件下能还原 Ag(NH3)2+:
4Ag(NH3)2++N2H4•H2O═4Ag↓+N2↑+4NH4++4NH3↑+H2O
-
(1)
“氧化”阶段需在 80℃条件下进行,适宜的加热方式为.
-
-
(2)
NaClO 溶液与 Ag 反应的产物为 AgCl、NaOH 和 O2 , 该反应的化学方程式为. HNO3也能氧化Ag,从反应产物的角度分析,以HNO3代替NaClO的缺点是.
-
-
(3)
为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并.
-
-
(4)
若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因过量NaClO与NH3•H2O反应外(该条件下NaClO3与NH3•H2O不反应),还因为.
-
-
(5)
请设计从“过滤Ⅱ”后的滤液中获取单质Ag的实验方案:(实验中须使用的试剂有:2mol•L﹣1水合肼溶液,1mol•L﹣1H2SO4 ).
-
