(14分)某混合物浆液含有Al(OH)3、MnO2和少量Na2CrO4 . 考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图),使浆液分离成固体混合物和含铬元素溶液,并回收利用.回答Ⅰ和Ⅱ中的问题.
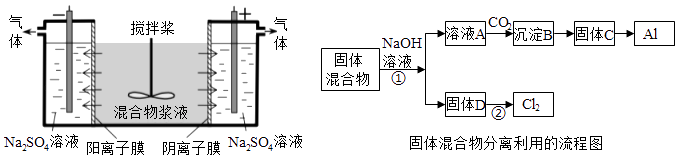
Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
-
(1)
反应①所加试剂NaOH的电子式为.B→C的反应条件为,C→Al的制备方法称为.
-
-
(2)
该小组探究反应②发生的条件.D与浓盐酸混合,不加热,无变化;加热有Cl
2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl
2 . 由此判断影响该反应有效进行的因素有(填序号)
.
a.温度 b.Cl﹣的浓度 c.溶液的酸度
-
-
(3)
0.1mol Cl
2与焦炭、TiO
2完全反应,生成一种还原性气体和一种易水解成TiO
2•xH
2O的液态化合物,放热4.28kJ,该反应的热化学方程式为
.
Ⅱ含铬元素溶液的分离和利用
-
-
(4)
用惰性电极电解时,CrO42﹣能从浆液中分离出来的原因是,分离后含铬元素的粒子是;阴极室生成的物质为(写化学式).
-
