根据以上信息回答下列问题:
|
pH |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
CuCl产率/% |
70 |
90 |
82 |
78 |
75 |
72 |
70 |
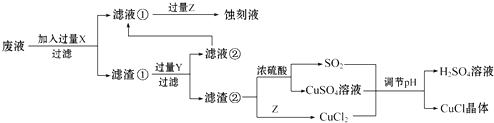
析出CuCl晶体最佳pH为,当pH较大时CuCl产率变低原因是.调节pH时,(填“能”或“不能”)用相同pH的硝酸代替硫酸,理由是.
①称取样品0.25g和过量的FeCl3溶液于锥形瓶中,充分溶解.
②用0.10mol•L﹣1硫酸铈标准溶液滴定.已知:CuCl+FeCl3═CuCl2+FeCl2、Fe2++Ce4+═Fe3++Ce3+ . 三次平行实验结果如下(平行实验结果相差不能超过1%):
|
平行实验次数 |
1 |
2 |
3 |
|
0.25g样品消耗硫酸铈标准溶液的体积(mL) |
24.35 |
24.05 |
23.95 |
则样品中CuCl的纯度为(结果保留三位有效数字).