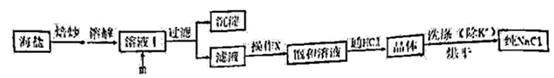
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳

①用浓硫酸和海盐混合加热制取氯化氢利用了浓硫酸的性质是(填编号),相比分液漏斗,选用仪器a的优点是。
a.高沸点 b.强酸性 c.强氧化性
②对比实验发现,将烧瓶中的海盐磨细可加快NaCl晶体的析出,其原因是。
| 操作 | 目的/结论 | |
| ① | 称取样品 | 目的:。 |
| ② | 过滤洗涤,干燥后称得沉淀为m2g | 结论:样品中SO |