已知:S+Na2SO3Na2S2O3
按如图所示装置(加热及夹持装置省略)进行实验,再经多步操作制得Na2S2O3﹒5H2O的粗产品![]()
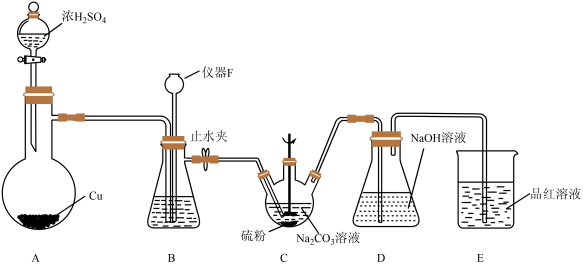
仪器F的名称为,装置B的作用之一是观察SO2的生成速率,其中的试剂最好选用。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
称取粗产品12.400g配制成100mL溶液,取25.00mL该溶液于锥形瓶中,用0.2500mol·L-1的I2标准液滴定,反应原理为:I2+2S2O→2I-+S4O
, 实验数据如表:
编号 | 初读数(mL) | 末读数(mL) |
① | 0.00 | 19.99 |
② | 1.00 | 21.01 |
③ | 1.00 | 23.00 |
用作为指示剂,滴定至终点时溶液的颜色由色变为色,且30s内溶液颜色不变。粗产品中Na2S2O3﹒5H2O的质量分数为。下列情况可能导致测量结果偏低的操作是 。
a.粗产品中Na2S2O3﹒5H2O失去部分结晶水
b.滴定前装I2标准液的滴定管未用标准液润洗
c.锥形瓶用蒸馏水洗净后未用待测液润洗
d.滴定时锥形瓶中有少量液滴溅出