①上述滴定操作用到的仪器有。
A. B.
B. C.
C. D.
D.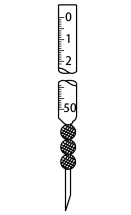
②该盐酸浓度为。
序号 | 反应试剂 | 体系温度/ | ||
反应前 | 反应后 | |||
i | | | a | b |
ii | | a | c | |
①温度:bc(填“>”“<”或“=”)。
②(选择表中一组数据计算)。结果表明,该方法可行。
查阅资料:配制溶液时需加入酸。加酸的目的是。
提出猜想:粉与
溶液混合,在反应A进行的过程中,可能存在
粉和酸的反应。
验证猜想:用试纸测得
溶液的
不大于1;向少量
溶液中加入
粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和(用离子方程式表示)。
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为。