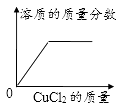
 B .
B . 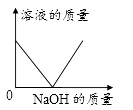 C .
C . 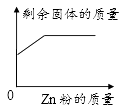 D .
D . 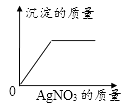
 横
B .
横
B .  平
C .
平
C . 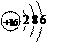 ,则S2-的电子数为。
,则S2-的电子数为。

A.NaCl
B.NaOH
C.CaO

A.将Sc投入CuSO4溶液中有红色物质析出
B.仅用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag能验证钪和铁的活动性强弱
C.仅用Fe、Sc、稀H2SO4溶液能验证钪和铁的活动性强弱
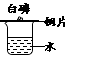
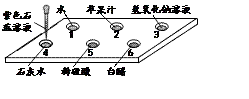
①反应的化学方程式为。
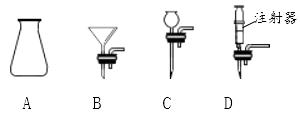
②实验中,为了得到平稳的气流,最适合的装置组合是(填序号)。
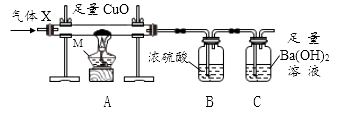
查阅资料:(ⅰ)加热时,CH4能与CuO反应生成Cu、CO2和H2O;
(ⅱ)20℃时,Ca(OH)2和Ba(OH)2溶解度分别为:0.165g、2.1g。
猜想1:只有CO 猜想2:只有CH4 猜想3:既有CO又有CH4
①实验时,先往装置中通一段时间的N2 , 再通入气体X后加热,实验中有下列变化:
变化1:A中玻璃管内黑色粉未逐渐变红 变化2:B瓶增重 变化3:C中出现浑浊
根据变化(填“1”“2”或“3”),可知猜想1不成立。
②根据上述变化仍无法确定气体X的成分,还需要测定(填序号),并进行定量分析才能得出结论。
a.实验前A中CuO的质量
b.B瓶增重的质量
c.C瓶增重的质量
①C中用Ba(OH)2溶液而不用Ca(OH)2溶液的原因是。
②从环保的角度,该装置还应进行的改进是。