①增大氢气的浓度 ②升高温度 ③降低温度 ④增大压强 ⑤增大HI的浓度 ⑥扩大体积 ⑦加催化剂.
①增大压强 ②增加炭的量 ③通入CO2 ④恒压下充入N2 ⑤恒容下充入N2 ⑥升温
 B .
B . 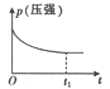 C .
C . 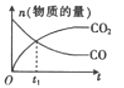 D .
D . 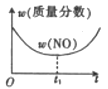
时间/min | 1 | 2 | 3 | 4 | 5 |
氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
反应速率最小的时间段是,原因为。

t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | C1 | C2 | C3 | C3 |
4 | C1 | C2 | C3 | C3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
①表中3min﹣4min之间反应处于状态;C1数值 0.08mol/L (填大于、小于或等于).
②反应在4min﹣5min问,平衡向逆方向移动,可能的原因是(单选),表中5min﹣6min之间数值发生变化,可能的原因是(单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
实验测得不同温度下的平衡数据列于下表: