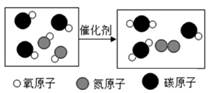

 B . 镁带燃烧
B . 镁带燃烧  C . 电解水
C . 电解水  D . 火药爆炸
D . 火药爆炸 
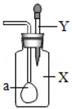
| X | Y | |
| A | CO | Ca(OH)2 溶液 |
| B | CO2 | NaOH 溶液 |
| C | HCl | Ca(OH)2 溶液 |
| D | SO2 | NaOH 溶液 |

实验操作 | 甲 | 乙 | 丙 | 丁 |
加入无色酚酞试液 | 不变色 | 变红 | 不变色 | 不变色 |
加入硝酸钡溶液 | 白色沉淀 | 无明显现象 | 白色沉淀 | 无明显现象 |
加入锌粒 | 无明显现象 | 无明显现象 | 产生无色气体 | 产生无色气体 |
则对应甲、乙、丙、丁顺序的四种物质是( )
 B .
B .  C .
C . 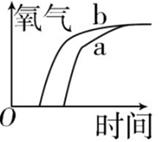 D .
D . 

①原子的数目 ②分子的数目 ③元素的种类 ④物质的种类 ⑤原子的种类⑥物质的总质量 ⑦元素的化合价
①稀盐酸 ②食醋 ③肥皂水 ④食盐水
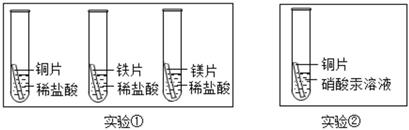
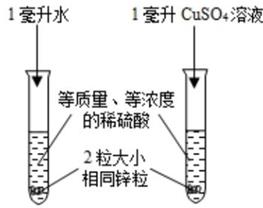
根据实验①判断出镁的金属活动性比铁强,依据的现象是,根据实验②判断反应后得到溶液的质量(填“>”或“<”或“=”)反应前溶液的质量。
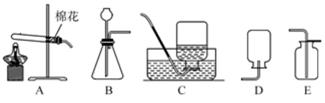
实验一:如图甲,将一支充满二氧化碳的试管倒扣在盛有氢氧化钠溶液的烧杯中,观察试管中的液面变化情况。
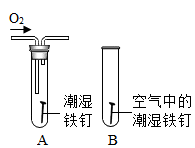
实验二:如图乙,向两个装满二氧化碳的同样规格的瓶中分别注入等量的氢氧化钠溶液和蒸馏水,振荡后放在水平的桌面上,观察 U 形管(装有红墨水)两端液面的变化情况,请问:


|
试管 |
A |
B |
C |
D |
E |
F |
|
CuSO4 溶液/毫升 |
0 |
0.5 |
1 |
1.5 |
2 |
4 |
|
水/毫升 |
4 |
3.5 |
3 |
V1 |
V2 |
0 |
|
收集 H2 所用的时间/秒 |
348 |
246 |
190 |
165 |
230 |
360 |
试管 D 中加入水的体积 V1=毫升;由上表可得出,CuSO4 的溶液的量对稀硫 酸与锌反应速率影响的变化趋势是。
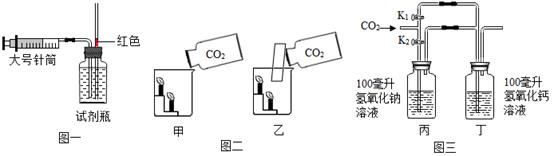
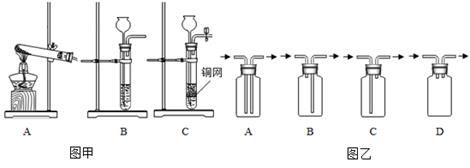
图一:探究 CO2 在水中的溶解能力。
①试剂瓶加满(填“蒸馏水”或“干净雨水”),恰好 200 mL,塞紧橡皮塞; ②用针筒抽取 200 mLCO2;连接装置,缓慢推动活塞,将 CO2 注入瓶内;
③当注入 CO2 气体体积达到 120 mL 时,红色油柱开始向上移动。则表明在该条件下,1
体积水中能溶解体积 CO2。
图二:验证 CO2 的密度比空气大,应选装置易成功。
图三:验证 CO2 能否与 NaOH、Ca(OH)2 反应。
①关闭 K1 , 打开 K2 , 缓缓通入 600 mL CO2 , 丙、丁容器中均无明显现象;
②打开 K1 , 打开 K2 , 继续通入 CO2 , 丁容器中出现浑浊。
根据上述现象,可推断 CO2。
A.一定能与 NaOH 反应 B.可能与 NaOH 反应
C.一定能与 Ca(OH)2 反应 D.可能与 Ca(OH)2 反应
Na2CO3 还是盐酸,小芳认为此方法不可行,原因是。
|
方案 |
加入试剂 |
分离方法 |
方案评价 |
|
1 |
适量 Ca(OH)2 溶液 |
过滤、蒸发、结晶 |
不可行,理由 是 |
|
2 |
过量的稀盐酸 |
蒸发结晶 |
可行 |
|
物质 |
a |
b |
c |
d |
|
反应前质量/g |
8.4 |
5.2 |
6.0 |
0.6 |
|
反应后质量/g |
待测 |
4.56 |
9.2 |
0.6 |
分析表中数据可知:



| 实验序号 | 1 | 2 | 3 |
| 碳酸氢钠片样品质量/克 | 3.0 | 3.0 | 3.0 |
| 反应前总质量/克 | 193.8 | 194.6 | 193.6 |
| 反应后总质量/克 | 192.6 | 193.6 | 192.5 |
| 二氧化碳质量/克 |
|
|
|
请计算药片中碳酸氢钠的质量分数。