 B . 门捷列夫
B . 门捷列夫  C . 拉瓦锡
C . 拉瓦锡  D . 侯德榜
D . 侯德榜 
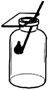 B . 检查装置气密性
B . 检查装置气密性 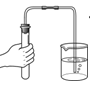 C . 点燃酒精灯
C . 点燃酒精灯 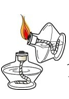 D . 稀释浓硫酸
D . 稀释浓硫酸 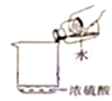
|
选项 |
A |
B |
C |
D |
|
常见物质 |
葡萄汁 |
牛奶 |
苹果汁 |
牙膏 |
|
pH |
3.5 —4.5 |
6.3—6.6 |
3.0 |
9.0 |
| 选 项 | 物 质 | 杂 质 | 除去杂质所选试剂 |
| A | 碳酸钙 | 氧化钙 | 盐酸 |
| B | 氯化钠溶液 | 碳酸氢钠 | 盐酸 |
| C | 一氧化碳 | 二氧化碳 | 氢氧化钠溶液 |
| D | 硝酸铜溶液 | 硝酸银 | 铜 |
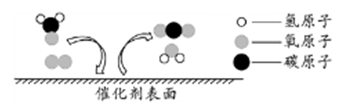



尿素,是一种白色晶体,化学式为CO(NH2)2 , 属于有机物,它是目前使用量最大的一种化学肥料。
尿素是蛋白质在体内代谢的产物。早在1737~1785年,德国医生博哈夫和法国实验员鲁埃分别通过蒸发尿液获得了尿素。
1811年,英国化学家戴维将一氧化碳和氯气(Cl2)的混合物暴露在日光中,获得光气(COCl2),再将光气与氨作用合成尿素。目前工业上用氨气和二氧化碳在一定条件下合成尿素。
尿素在土壤中酶的作用下,转化成碳酸铵或碳酸氢铵,才能被作物吸收利用,在土壤中不残留任何有害物质,长期施用没有不良影响。尿素在转化前是分子态的,不能被土壤吸附,应防止随水流失。
依据文章内容,回答下列问题:

① 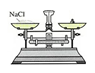 ②
②  ③
③ 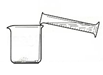 ④
④  ⑤
⑤ ![]()
| A | B |
| ⑴①中称量氯化钠的质量为g。 ⑵④中玻璃棒的作用是。 | ⑴③中量取水的体积是mL。 ⑵填写⑤中标签 |
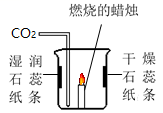

 C . 黄金首饰
C . 黄金首饰 

|
清洁剂 |
| | |
| 名称 | 洁厕灵 | 彩漂液 | 漂白水 |
| 有效成分 | HCl | H2O2 | NaClO(次氯酸钠) |
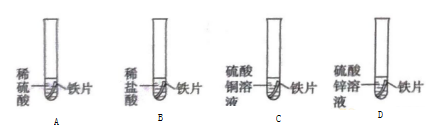
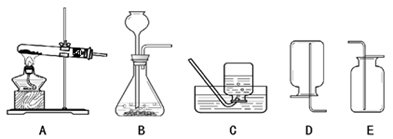
A 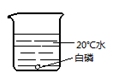 B
B 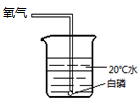 C
C 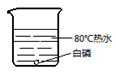 D
D 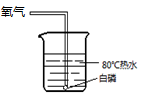

|
氧气体积分数(%) |
30 |
40 |
60 |
70 |
|
带火星的木条 |
不变 |
稍亮 |
复燃 |
复燃 |
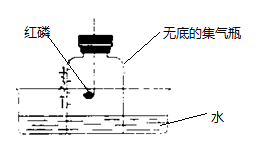
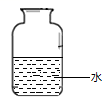
根据上述实验数据得出的结论是 。在集气瓶中注入占其容积50%的水(如图所示),用排水法收集氧气,将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,推测实验现象并说明理由。。

(查阅资料)
①几种常见铁的氧化物的颜色、状态及能否被磁铁吸引如下表所示。
|
常见铁的氧化物 |
FeO |
Fe2O3 |
Fe3O4 |
|
颜色、状态 |
黑色粉末 |
红棕色粉末 |
黑色晶体 |
|
能否被磁铁吸引 |
否 |
否 |
能 |
②四氧化三铁能与稀硫酸反应:Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
(初步实验验证)
试管中剩余固体为黑色,能全部被磁铁吸引,则剩余固体一定不含氧化物、。
猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是。
|
实验操作 |
实验现象 |
实验结论 |
|
取少量黑色固体于试管中,滴加足量的稀硫酸。 |
|
猜想一不成立, 猜想二成立。 |
(查阅资料)①碘单质(I2)遇淀粉液变蓝。②部分酸、碱、盐通常在水溶液中以离子形式存在,如:盐酸中存在H+和Cl-。
(进行实验)
实验1 将不同浓度的KI溶液置于纯氧中,放置相同时间后观察,现象如下表:
|
装置 |
烧杯中的液体 |
现象 |
|
| ①2 mL 0.15%KI溶液+5滴淀粉液 | 无明显变化 |
| ②2 mL 1.5%KI溶液+5滴淀粉液 | 溶液变蓝 | |
| ③2 mL 15%KI溶液+5滴淀粉液 | 溶液变蓝,颜色较②深 |
实验2 将相同浓度的KI溶液加入不同浓度的稀盐酸后置于纯氧中,5分钟后观察,现象如下表:
| 装置 | 烧杯中的液体 | 现象 |
| | ④ 2 mL 15%KI溶液+5滴淀粉液+2mL蒸馏水 | 无明显变化 |
| ⑤ 2 mL 15%KI溶液+5滴淀粉液+2 mL1% 盐酸 | 溶液变蓝 | |
| ⑥ 2 mL 15%KI溶液+5滴淀粉液+2 mL 10% 盐酸 | 溶液变蓝,颜色较⑤深 |
实验1的目的是。
实验④中加2mL蒸馏水的作用是。