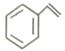
 分子中所有原子不可能处于同一平面
D . 用碳酸钠溶液不能一次性鉴别乙酸、苯和乙醇三种无色液体
分子中所有原子不可能处于同一平面
D . 用碳酸钠溶液不能一次性鉴别乙酸、苯和乙醇三种无色液体
实验 | 现象 | 结论 | |
A | 某溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 原溶液中有Fe2+ , 没有Fe3+ |
B | 将红热的木炭投入浓硫酸中产生的气体通入澄清的石灰水 | 石灰水变浑浊 | 木炭化成CO2 |
C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
D | 将0.1mol/L的NaCl溶液滴入硝酸银溶液至不现有沉淀产生,再滴加0.1mol/L KI溶液 | 先有白色沉淀生成,后变黄色沉淀 | Ksp(AgCl) >Ksp(AgI) |
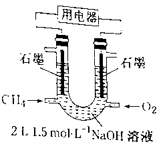
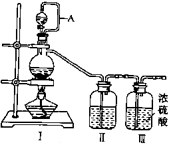
①写出利用装置Ⅰ制备氯气的离子反应方程式:。
② 利用上述装置制备NO时,Ⅱ中盛装物质为(写化学式)。

①装置连接顺序为a→按气流自左向右方向,用小写字母表示)。
②为使NO和Cl2恰好完全反应生成CNO,理论上通入NO和Cl2 , 两种气体的流速比为。
③装置Ⅸ的作用是。
④装置吸收尾气,有同学认为尾气中的某种气体不能完金被吸收。为了充分吸收尾气,可将尾气与(气体)同时通入NaON溶液中。
⑤王水是浓盐酸和浓硝酸的混酸,一定条件下混酸可生成ClNO和Cl2 , 该反应的化学方程式为。
⑥写出验证ClNO与H2O完全反应后的溶液中存在Cl-和HNO2的实验步骤:取少量反应后的溶液于试管中,。(限选试剂如下:AgNO3溶液,稀硝酸,KMnO4溶液)


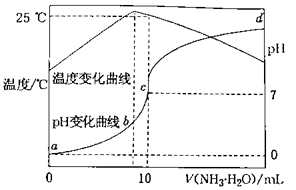
若在压强p1下达到化学平衡状态A时,容器的体积为10L。如果反应开始时仍充入2molCO和4molH2 , 则在压强p2下达到平衡状态B时容器的体积V(B)=L。
|
GaN |
GaP |
GaAs |
|
|
熔点 |
1700℃ |
1480℃ |
1238℃ |

①品胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为:
②GaN的密度为g·cm-3(用a、NA表示)。
①有两种官能团
②遇FeCl3溶液显紫色
③ 核磁共报氢谱有五组峰,峰面积之比是3:2:2:2:1