 B . 滴加液体
B . 滴加液体  C . 加热固体药品
C . 加热固体药品  D . 量取9.5mL液体
D . 量取9.5mL液体 

| 选项 | 物质(括号内为杂质) | 除杂试剂 | 操作方法 |
| A | NaCl(Na2SO4) | 过量BaCl2溶液 | 过滤 |
| B | K2CO3(KCl) | 足量稀盐酸 | 蒸发结晶 |
| C | N2(CO) | CuO | 通过灼热的CuO |
| D | KNO3(NaCl) | 水 | 加热溶解、降温结晶 |



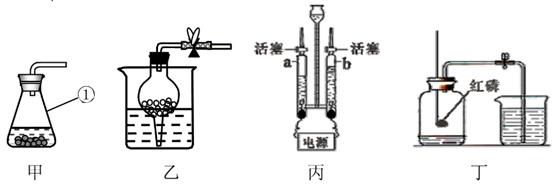
①结合上图分析,化学变化中的最小粒子是(选填“分子”、“原子”或“离子”,下同),丙图中所示物质都是由 构成的。
②该反应的化学方程式是 。


(已知:Ⅰ.SiO2不溶于水、不与硫酸反应。Ⅱ.转化率是反应物转化为生成物的百分率。)

(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为℃。

【查阅资料】
① 在标准状况下,氧气的密度是1.429g/L。在室温下,1L水中能溶解约30mL的氧气。
② 过氧化钠能与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O2
③ 过氧化钠能与水反应:2Na2O2+2H2O=4NaOH+O2↑
④BaCl2溶液呈中性。
【成分猜想】固体中可能有Na2O2、NaOH和Na2CO3中的一种或几种。
|
实验步骤 |
实验现象 |
结论或化学方程式 |
|
①取少量样品于试管中,加水溶解, 并立即将带火星的木条伸入试管中。 |
有气泡产生, |
证明固体中含有Na2O2。 |
|
②取步骤①所得溶液于试管中,滴加过量的BaCl2溶液。 |
有白色沉淀生成。 |
证明固体中含有Na2CO3 , 化学方程式为 |
|
③取步骤②中的上层清液于试管中,滴入1~2滴酚酞试液。 |
溶液变红 |
证明固体中含有NaOH。 |

①装置乙中植物油的作用是 。
②待反应完全后,根据收集所得气体的体积,进行相关计算,得出样品中 的质量。
③再将烧瓶中的沉淀进行过滤、洗涤、烘干、称量,进行相关计算,得出样品中的质量。
