 禁止吸烟
B .
禁止吸烟
B .  禁止燃放鞭炮
C .
禁止燃放鞭炮
C .  禁止放易燃物
D .
禁止放易燃物
D .  禁止烟火
禁止烟火


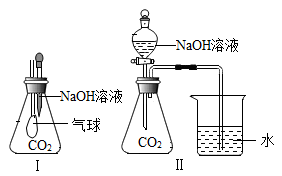
①选择装置I时,可观察到的实验现象为:。
②选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的原因是:。
③CO2和NaOH溶液反应的化学方程式为。

(查阅资料)
a.碱式碳酸亚铁受热会完全分解生成FeO、CO2以H2O。
b.FeO是一种黑色粉末,它不稳定,在空气中加热,可被氧化成四氧化三铁。
c.碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
(实验步骤)
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 200.36 | 180.88 | 180.00 |
分析图、表中数据可知:3.40g碱式碳酸亚铁受热分解过程中生成H2O的质量为g,CO2的质量为g,装置E的作用是。
在xFeCO3•yFe(OH)2•zH2O中,氢原子与氧原子的个数之比为。
①装置A的作用是。
②实验结束后,装置B中的残留固体可能全部是FeO.也可能全部是Fe3O4 . 还可能是。
③为了得到装置B中残留固体的组成,华雪同学称得装置B中残留固体质量为2.24g后,通过计算可知:残留固体的组成及各成分的质量为。