①0.5 mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠

 B .
B .  C .
C . 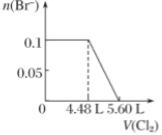 D .
D . 
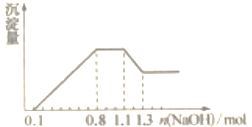
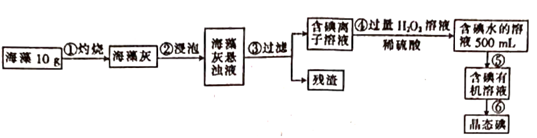
①上述流程中涉及下列操作,其中错误的是(填标号)

②写出步骤④发生反应的离子方程式: 。
③要证明步骤④所得溶液中含有碘单质,可加入(填试剂名称),观察到 (填现象)说明溶液中存在碘。
①Fe粉与稀硝酸反应生成硝酸铁的化学方程式为 。
②反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+)=。
③标准状况下,生成NO气体的体积为 L(保留两位小数)。