 B . 植物进行光合作用
B . 植物进行光合作用  C . 铁丝变形
C . 铁丝变形  D . 氯化铁溶液中加硫氰化钾溶液
D . 氯化铁溶液中加硫氰化钾溶液 
| 物质 | 酸奶 | 鸡蛋清 | 牙膏 | 肥皂水 |
| pH范围(常温) | 4~5 | 7~8 | 8~9 | 10~11 |
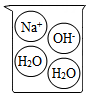 B .
B . 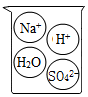 C .
C . 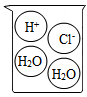 D .
D . 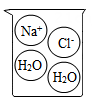
 加热液体
B .
加热液体
B .  测试溶液Ph
C .
测试溶液Ph
C . 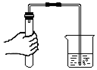 气密性检查
D .
气密性检查
D . 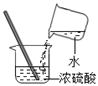 稀释浓硫酸
稀释浓硫酸
| 药品柜编号 | ① | ② | ③ | ④ | …… |
| 药品 | 氢氧化钠 氢氧化钙 | 盐酸 硫酸 | 二氧化锰 氧化铜 | 氯化钠 硫酸钠 | …… |
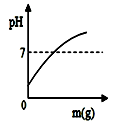 B .
B .  C .
C . 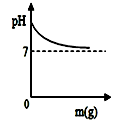 D .
D . 
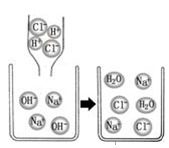
①无色酚酞试液 ②紫色石蕊试液 ③pH试纸
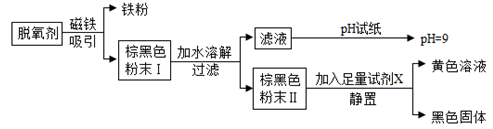
①纯净的氢氧化钾是白色固体;②氢氧化钾极易溶解于水;③氢氧化钾固体露置于空气中易吸水而潮解;④氢氧化钾和氯化铁溶液混合可以制得氢氧化铁。
根据上面短文的内容,运用你学过的有关知识填空:

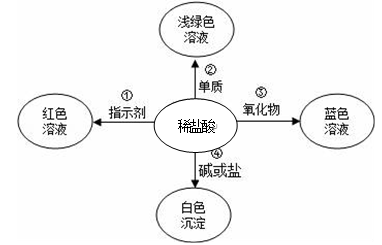


①取5毫升试剂于A试管中,滴入几滴无色酚酞试液,无色酚酞试液
②另取5毫升试剂于B试管中,滴入几滴氯化钡溶液,溶液中出现白色沉淀。
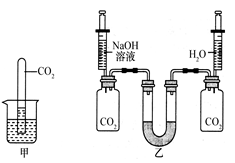
实验一:如图甲,将一支充满二氧化碳的试管倒扣在盛有氢氧化钠溶液的烧杯中,观察试管中的液面变化情况。
实验二:如图乙,向两个装满二氧化碳的同样规格的瓶中分别注入等量的氢氧化钠溶液和蒸馏水,振荡后放在水平的桌面上,观察U形管(装有红墨水)两端液面的变化情况。请问:
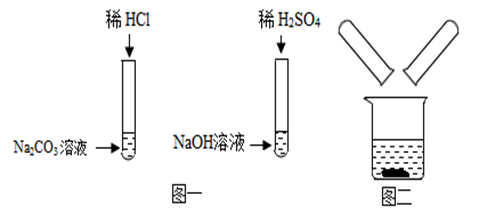
【查阅资料】Na2SO4溶液、NaCl溶液呈中性。
【提出猜想】猜想1:Na2SO4、NaCl;
猜想2: Na2SO4、NaCl和 ? ;
猜想3:Na2SO4、NaCl和H2SO4;
【进行实验】小明同学设计如下两个实验方案:
| 实验步骤 | 实验现象 | 实验结论 | |
| 方案一 | 取少量烧杯中的溶液于洁净的试管中,加入几滴紫色石蕊溶液 | ⑴ | 猜想3正确 |
| 方案二 | 取少量烧杯中的溶液于洁净的试管中,加入少量锌粒 | ⑵ |
【反思与总结】分析反应后溶液中溶质成分,除要考虑生成物外,还需考虑反应物是否过量。
⑶猜想2中“?”处应填(化学式)。
|
冲泡菊花的水 |
煮沸的井水(弱碱性) |
煮沸的纯净水中滴有白醋 |
煮沸的纯净水 |
|
变色情况 |
变浅绿色 |
变浅绿色 |
几乎不变色 |
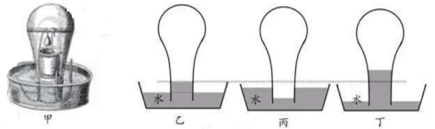
Ⅰ.将一根长度等于玻璃钟罩最宽部分直径的铁棒横放在钟罩里,把装有稀硝酸的陶罐通过铁钩挂在铁棒上,用绳索将小铁块悬挂在陶罐的正上方(铁块的升降通过在钟罩外拉动或放松绳索来实现)。
Ⅱ.调整水槽中初始水位如图乙,再使铁块浸入稀硝酸中,观察到铁块表面迅速产生大量气泡,钟罩内水面下降。[稀硝酸有强氧化性,能与铁发生如下反应:4HNO3+Fe=Fe(NO3)3+NO↑+2H2O
Ⅲ.当水位降至接近钟罩口时(如图丙),立即取出铁块,以防气体外逸。
IV.等待一段时间后,水面稳定在如图丁的位置。(一氧化氮会与氧气等物质发生如下反应:4NO+3O2+2 ? =4HNO3)
分析与评价:

|
加入稀盐酸的体积/mL |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
|
烧杯中溶液的pH |
12.9 |
12.7 |
12.5 |
12.3 |
11.9 |
7.0 |
2.1 |
1.9 |
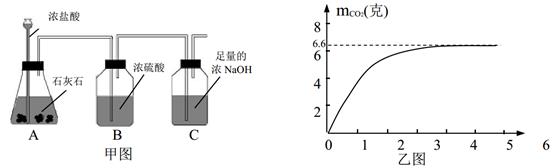
①用天平准确称取20克石灰石放入甲图A装置中,同时加入足量浓盐酸;
②测量C装置中吸收到的二氧化碳的质量,并据此绘成乙图中的曲线;
③根据实验结果计算该石灰石的纯度。
请分析回答下列问题:(CaCO3+2HCl=CaCl2+CO2↑+H2O)
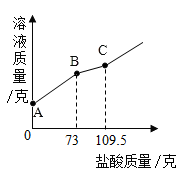
Na2CO3+2HCl=2NaCl+H2O+CO2↑ NaOH+HCl=NaCl+H2O