 振荡试管
C .
振荡试管
C .  氧气验满
D .
氧气验满
D .  测酸碱度
测酸碱度
①若用氯化钠固体配制,需称取氯化钠固体7.0g
②选用200mL量筒量取所需水的体积
③实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和试剂瓶
④用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏小.
物质 | 杂质(少量) | 试剂 | 操作方法 | |
A | 氯化钙固体 | 熟石灰 | 过量稀盐酸 | 蒸发结晶 |
B | H2 | HCl | 适量的饱和碳酸氢钠溶液 | 洗气 |
C | 硝酸 | 盐酸 | 过量的硝酸银溶液 | 过滤 |
D | FeSO4溶液 | CuSO4溶液 | 过量的Fe | 过滤 |
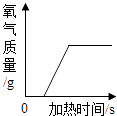 加热一定质量的高锰酸钾
B .
加热一定质量的高锰酸钾
B . 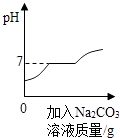 向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液
C .
向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液
C . 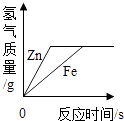 向等质量等质量分数的稀盐酸中分别加入过量的锌和铁
D .
向等质量等质量分数的稀盐酸中分别加入过量的锌和铁
D . 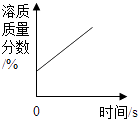 将一瓶浓硫酸敞口放置在空气中
将一瓶浓硫酸敞口放置在空气中
①两个汞原子②三个氯离子
③海水中含量最多的金属元素④氧化亚铜中铜元素化合价为+1价
⑤6个葡萄糖分子⑥缺元素会导致侏儒症
a.K2CO3b.KNO3c.CH4d.Fe2O3e.NaHCO3
①可用作发酵粉的是②草木灰的主要成分
③用作复合肥的是④可以做燃料的物质.
Ⅰ.关于雪碧的研究.
资料一:市场目前所售“雪碧”汽水的包装,主要有图1A、B、C三图所示:
品名雪碧汽水(清爽柠檬味汽水)
配料:水、白砂糖、食品添加剂(二氧化碳、柠檬酸、柠檬酸钠、苯甲酸钠)、食用香精 等
保质期:9个月
保存方法:禁止加热或0℃以下冷冻、避免阳光直晒或高温

资料二:柠檬酸为白色固体,化学性质稳定.
(1 )实验一:小明将鸡蛋浸入白醋中(如图2所示),白醋中醋酸化学式用HAc表示(其中Ac代表醋酸根),请您写出蛋壳与醋酸反应方程式:;
(2 )实验二:取蛋壳用镊子夹取后,在家庭煤气灶火焰上灼烧,请回答以下问题:
①一会儿蛋壳内侧就变黑,同时产生烧焦羽毛的气味,说明蛋壳内侧的“凤凰衣”含有的营养物质是;
②一段时间后将灼烧后的“蛋壳”放入装有少量水的玻璃杯中,向其中加入一片“果导”(主要成分为酚酞),此时出现的现象为;静置后,取上层清液向其中吹气,可观察到.
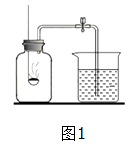
①实验原理:(用化学方程式表示).
②实验步骤:先用弹簧夹夹住橡皮管,点燃红磷,伸入瓶中并塞上瓶塞.等红磷燃烧熄灭后再打开弹簧夹.
③误差分析:发现实验结论大于理论值,可能的原因有.
A.装置漏气
B.实验时使用的红磷过量
C.实验时插入燃烧匙的速度太慢,集气瓶内部分空气受热逸出
D.红磷熄灭后没等集气瓶冷却就立刻打开弹簧夹
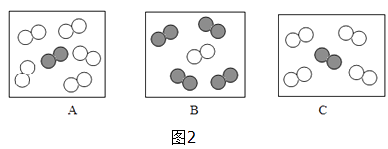
①用“ ![]() ”可表示的微粒是(填名称).
”可表示的微粒是(填名称).
②同温同压下,气体的体积比等于分子数目比.若空气中其它成分忽略不计,图2可表示空气微观模型的是(填标号).
已知:常压下,氮气沸点﹣196℃,氧气沸点﹣183℃.将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是.将该烧杯放置一段时间后,液态物质剩余约 体积,其主要成分是.

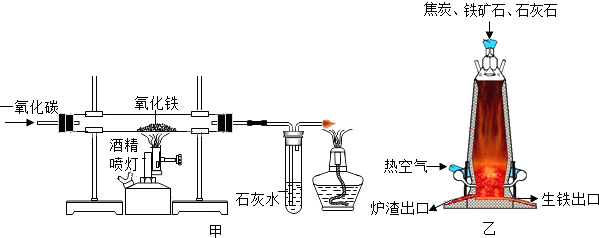
①Ⅰ中参加反应的单质甲为.
②Ⅱ中反应的化学方程式为.
③物质所含元素化合价发生变化的反应称为氧化还原反应.反应Ⅲ(填“属于”或“不属于”)氧化还原反应.
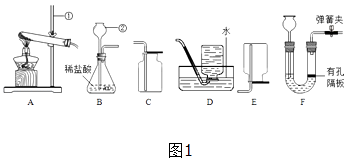
A.从水中取出导气管B.熄灭酒精灯
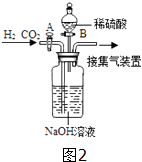
①关闭活塞B,打开活塞A,通入混合气体,可收集到气体.
②然后,(填操作),又可收集到另一种气体.
资料1:NaHCO3+NaOH=Na2CO3+H2O
资料2:碳酸钠和碳酸氢钠的溶解度表(一个标准大气压下)(部分)
温度/℃ | 0 | 15 | 20 | 30 | 40 | 50 | 60 |
碳酸氢钠溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 | 12.7 | 14.45 | 16.4 |
碳酸钠溶解度/g | 7.7 | 13.25 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
学校实验小组验证反应原理,在室温为15℃时,同学们将10g氢氧化钠固体完全溶解溶于80g水中(见图1烧杯),而后匀速的通入二氧化碳气体.同时用传感器测定溶液的pH变化,同时用数据采集器记录并绘制图象如图2所示.
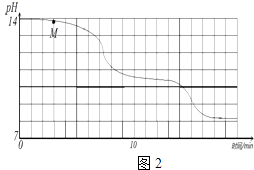
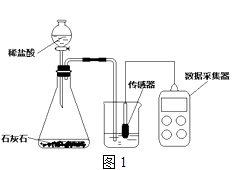
实验步骤 | 加入试剂 | 实验现象 | 初步实验结论 |
① | 加入 | 有白色沉淀 | 有物质 |
② | 滴入 |
|
Ⅰ.聚合硫酸铁的工业生产.
如图是以回收废铁屑为原料制备PFS的一种工艺流程.

回答下列问题
A.KMnO4B.Cl2C.H2O2D.HNO3
该研究小组为确定聚合硫酸铁的化学式,进行了如下实验:
①称取5.52g聚合硫酸铁样品溶于足量的稀盐酸中并充分混合;
②向①所得的混合物中加入足量的BaCl2溶液,充分反应后,经过滤、洗涤、干燥、称重,得沉淀4.66g.
③若向步骤②的滤液中加入过量的NaOH溶液,充分反应后,再将沉淀过滤、洗涤、灼烧、称重,得固体3.20g.
则聚合硫酸铁[Fex(OH)y(SO4)z]m样品中的x:y:z的值为.
试写出该聚合硫酸铁与盐酸的反应方程式.
该小组将5.52g聚合硫酸铁在一定条件下加热完全分解,对所得气体产物进行实验探究.(已知SO3的熔点为16.8℃).
【提出假设】
假设1:所得气体的成分是SO3;
假设2:所得气体的成分是SO2、O2;
假设3:所得气体的成分是.
按下图装置进行实验.

实验过程中发现:B中无水硫酸铜变蓝,C中U形管内有无色晶体析出,D中品红溶液褪色,装置E的作用是.
【实验结论】
通过实验现象判断,假设成立.
如果最终试管中固体为一种红棕色纯净物,则质量为.