 B .
B .  C .
C .  D .
D . 



 B .
B .  C .
C .  D .
D . 
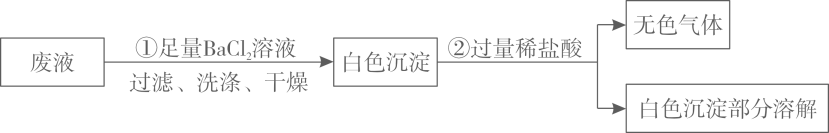
根据以上实验现象分析,可以得出原废液中( )

| 选项 | 实验操作 | 实验目的或结论 |
| A | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 说明该钾盐一定是KHCO3 |
| B | 向NaOH和Ca(OH)2混合溶液中加入过量的Na2CO3溶液后过滤 | 得到纯净的NaOH溶液 |
| C | 把2根铜丝分别浸入FeCl2溶液和AgNO3溶液 | 比较Fe、Cu、Ag的金属活动性 |
| D | 将NaNO3HCl、CaCl2和KOH四种溶液互相反应 | 鉴别四种溶液 |


①Si+O2 SiO2
②SiO2+Na2CO3 Na2SiO3+CO2↑
③SiO2+2C Si+2CO↑
④ Si+2NaOH+H2O Na2SO3+2H2↑




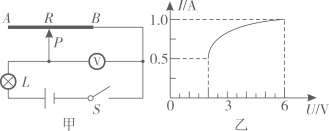
第一次:先在试管中加入2mL氢氧化钙溶液,再滴加氯化铁溶液,马上出现沉淀第二次:先在试管中加入2mL氯化铁溶液,再滴加氢氯化钙溶液,没有马上出现沉淀。


| 实验序号 | 铁块质量m/g | 铁块距桌面高度H/cm | 桌腿进入沙子的深度h/cm |
| ① | 20 | 20 | 1 |
| ② | 20 | 30 | 2.9 |
| ③ | 20 | 40 | 3.8 |
| ④ | 30 | 20 | 2.9 |
| ⑤ | 40 | 20 | 4.1 |
实验1:探究H2O2溶液浓度、温度对分解速率的影响
【实验方案】在一定温度下,向相同质量的H2O2溶液中加入相同质量的MnO2粉末,测量收集150mLO2所需的时间。
为了达到实验1的目的,需要补全实验方案。若a与b不相等,则a=。
|
实验序号 |
H2O2溶液的浓度% |
温度/℃ |
时间/s |
|
Ⅰ |
30 |
20 |
待测 |
|
Ⅱ |
15 |
30 |
待测 |
|
Ⅲ |
a |
b |
待测 |
【实验结论】实验发现H2O2分解速率与H2O2溶液的浓度和温度有关。
实验2:探究催化剂对反应速率的影响
【发现问题】小科在实验过程中不小心将过氧化氢溶液滴到水泥板上,发现有大量气泡产生。
【建立猜想】水泥块能作过氧化氢分解的催化剂。
【实验验证】
|
实验步骤 |
实验现象 |
|
|
实验一 |
将带火星的木条伸入装有过氧化氢溶液的试管中 |
木条不复燃 |
|
实验二 |
在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 |
木条复燃 |
【结论】实验一:常温下过氧化氢溶液分解很慢。
实验二: 。
【讨论与反思】小敏认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,他觉得需要增加一个探究实验。
实验步骤Ⅰ:准确称量水泥块质量。
实验步骤Ⅱ:完成实验二。
实验步骤Ⅲ:待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、称量。
实验步骤Ⅳ:对比反应前后水泥块的质量。
但老师指出:要证明小科的猜想,小敏的补充实验还存在不足之处,需要再补充一个实验,目的是探究。


|
次数 |
1 |
2 |
3 |
4 |
|
加入硫酸铜溶液的质量/g |
25 |
25 |
25 |
25 |
|
剩余固体的质量/g |
10.2 |
10.4 |
10.6 |
10.6 |



第二次实验只比第一次实验减少4g纯碱样品,其他药品质量和实验方法均与第一次实验相同,过滤后,发现最终示数也是187.10g。第三次实验只比第二次实验增加50g氯化钙溶液,其他药品质量和实验方法与第二次实验相同,过滤后,发现最终示数还是187.10g求(计算结果精确到0.1%):
