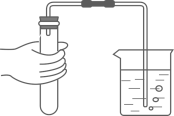
 B . 加入锌粒
B . 加入锌粒  C . 加入稀硫酸
C . 加入稀硫酸  D . 收集氢气
D . 收集氢气 
| 温度/℃ | 0 | 20 | 40 | 60 |
| NaCl的溶解度/g | 35.7 | 36.0 | 36.6 | 37.3 |
| KNO3的溶解度/g | 13.3 | 31.6 | 63.9 | 110 |


①图中碱性最强的体液是。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平(主要成分为Al(OH)3)治疗,其原理是(用化学方程式表示)。
84消毒液
(产品特点)主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.1%~6.9%。
(餐具消毒)用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。
(注意事项)①外用消毒剂,须稀释后使用。
②不得将本产品与酸性产品(如洁厕类清洁产品)同时使用。
依据表中信息,将有效氯的质量分数为6.0%的84消毒液与水按质量比为1:进行稀释,即可用于餐具消毒。洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整: 2HCl+NaClO=+Cl2↑+H2O。
|
实验内容 |
现象 |
说明、解释或结论 |
|
⑴用高锰酸钾制取氧气。 连接仪器,检查装置气密性。用(填仪器名称)取少量高锰酸钾装入试管中,并在试管口放一团棉花,固定好装置,加热试管,用排水法收集O2。 |
当观察到时,开始收集气体。 |
收集O2之前,将集气瓶内空气完全排净的方法是。产生O2的化学方程式为。 |
|
⑵酸与碱发生中和反应。 i.取少量稀NaOH溶液于试管中,滴入2滴酚酞溶液,再逐滴加入稀盐酸,边滴边振荡,至溶液的颜色恰好变为无色。 ii.往上述无色溶液中再滴入1滴稀NaOH溶液,观察现象。 |
步骤ⅱ中观察到。 |
步骤i中“边滴边振荡”的目的是。 |
用NaOH固体配制20g20%NaOH溶液,无需用到的玻璃仪器有___(填标号)。

实验前U型管两端液面相平,将NaOH溶液滴入试管中,恢复到室温后,U型管中的液面左高右低。据此,甲同学得出“CO2与NaOH发生了化学反应”的结论。
U型管中液面高度发生变化的原因是。

查阅资料:i.CaCl2溶液呈中性;ii.
实验步骤如下:
①检查装置的气密性,往装置中加入药品;
②关闭K1、K2 , 将注射器中的NaOH溶液缓缓推入A中;
③A中物质充分作用后,打开K1 , B中无色溶液倒吸入A中,A中产生沉淀且溶液显红色
④关闭K1 , 打开K2 , 将注射器活塞向上拉,C中溶液倒吸入A中。
步骤③“产生沉淀”的现象仍不足以证明CO2与NaOH发生了化学反应,理由是。