 闻气体气味
B .
闻气体气味
B . 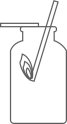 氧气验满
C .
氧气验满
C . 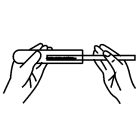 取用固体粉末
D .
取用固体粉末
D . | 选项 | 实验目的 | 实验操作 |
| A | 鉴别集气瓶中的O2和N2 | 分别将燃着的木条伸入集气瓶中,观察现象 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发结晶 |
| C | 检验某固体物质是否是铵盐 | 取样,加入少量熟石灰粉末,混合、研磨,观察是否放出刺激性气味的氨气 |
| D | 分离KCl和BaCl2的混合溶液 | 加入过量的Na2CO3溶液,过滤,洗涤,再分别向滤渣和滤液中加适量的稀盐酸 |


同学们经过讨论后认为猜想Ⅰ不正确,其理由是。
|
实验步骤 |
实验现象 |
实验结论 |
|
取少量溶液M于试管中,滴加紫色石蕊溶液 |
溶液显色 |
猜想Ⅱ正确 |
|
实验步骤 |
实验现象 |
实验结论 |
|
取少量溶液M于试管中,滴加硝酸银溶液和稀硝酸 |
产生白色沉淀 |
猜想Ⅲ正确 |
(分析评价)同学们对小强的实验方案进行了分析,认为他的实验结论不正确。如果猜想Ⅱ正确,按照方案二的实验操作,也会生成白色沉淀,此时发生反应的化学方程式为。
(再次探究)如果要验证猜想Ⅲ正确,可以设计实验方案三:取少量溶液M于试管中,然后分别加入下列物质进行实验,能观察到明显现象并得出正确结论的是(填序号)。
①锌粒 ②铜丝 ③二氧化碳 ④氧化铁 ⑤氢氧化钾 ⑥硫酸铜 ⑦碳酸钙 ⑧硝酸铵
(拓展应用)若将等质量、等质量分数的氢氧化钾溶液与硝酸溶液混合,充分反应,则所得溶液中含有的溶质是。