
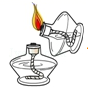
 C . 倾倒液体
C . 倾倒液体 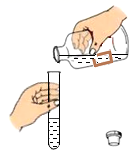 D . 读液体体积
D . 读液体体积 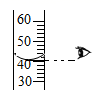

①计算:20℃时,将67g的KCl饱和溶液稀释为20%,需加水18g。
②量取:用量筒量取水倒入烧杯中,提供的量筒规格有10mL、20mL、50mL,应该选择mL的量筒。
③混匀:用搅拌,使溶液混合均匀。
A 40℃时,KNO3的溶解度是64g,表示100gKNO3饱和溶液中含64gKNO3
B Ca(OH)2的溶解度受温度变化的影响小于KCl的溶解度受温度变化的影响
C KNO3混有少量KCl时,可用降温结晶法提纯
D 60℃时,将等质量的KNO3、KCl两种物质分别配制成饱和溶液,KNO3需要水的质量大于KCl
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
VIA |
VIIA |
0 |
|
一 |
1H氢 |
2 He氦 |
||||||
|
二 |
3Li锂 |
4 Be铍 |
5B硼 |
6C碳 |
7N氮 |
8O氧 |
9F氟 |
10Ne氖 |
|
三 |
11Na钠 |
12Mg镁 |
13Al铝 |
14Si硅 |
15P磷 |
16S硫 |
17Cl氯 |
18Ar氩 |

(查阅资料)Ca(OH)2微溶于水,Cu(OH)2不溶于水。
(猜想与假设)猜想一:全部是Ca(OH)2
猜想二:全部是Cu(OH)2
猜想三:
小东从物理性质进行分析后认为猜想不合理,理由是。
|
实验 |
实验操作 |
实验现象 |
实验结论 |
|
实验Ⅰ |
取少量蓝色滤渣放入烧杯中,加入适量的水溶解后过滤,将滤液分成两等份,向其中一份滴入酚酞试液 |
滴入酚酞后滤液呈色 |
滤液显碱性,证明滤液中有OH-离子 |
|
实验Ⅱ |
向实验I的另一份滤液中滴入Na2CO3溶液 |
有白色沉淀 |
证明滤液中 有离子 |