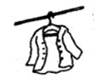
 B . 带火星的木条复燃
B . 带火星的木条复燃 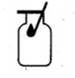 C . 食盐水的蒸发
C . 食盐水的蒸发 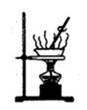 D . 灯泡通电发光
D . 灯泡通电发光 
| 农作物 | 大豆 | 茶 | 玉米 | 马铃薯 |
| pH | 6.0~7.0 | 5.5~5.5 | 7.0~8.1 | 4.8~5.5 |
 稀释浓硫酸
B .
稀释浓硫酸
B .  分离出AgNO3溶液中的AgCl
C .
分离出AgNO3溶液中的AgCl
C .  检查装置的气密性
D .
检查装置的气密性
D .  收集氧气
收集氧气


 B .
B .  C .
C .  D .
D . 
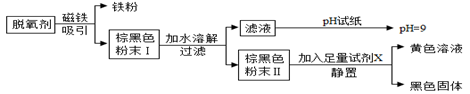
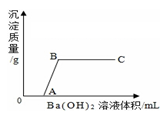

【猜想】猜想一:可能是NaCl和NaOH;猜想二:可能只有NaCl;
猜想三:
【进行实验】
|
实验步骤 |
实验操作 |
实验现象 |
结论 |
|
① |
取少量烧杯内的溶液于试管中,滴入几滴酚酞试液,振荡 |
|
猜想一不成立 |
|
② |
取少量烧杯内的溶液于另一支试管中,滴加碳酸钠溶液 |
|
猜想三成立 |
【对固体猜想】猜想I:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:是NaOH和Na2CO3混合物。
【实验和推断】

则该实验(填“能”或“不能”)说明猜想Ⅱ成立。
查阅资料:钠常温下就能与水发生剧烈反应,反应方程式为2Na+2H2O===2NaOH+H2↑。
提出猜想:猜想一:金属钠和硫酸铜溶液反应会有铜生成。
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜。
实验及现象:切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表所示:
|
编号 |
钠块大小 |
硫酸铜溶液 |
实验中产生沉淀的现象 |
|
① |
绿豆大小 |
稀溶液10毫升 |
产生蓝绿色沉淀 |
|
② |
绿豆大小 |
浓溶液10毫升 |
产生蓝色絮状沉淀 |
|
③ |
豌豆大小 |
稀溶液10毫升 |
产生蓝色絮状沉淀 |
|
④ |
豌豆大小 |
浓溶液10毫升 |
产生蓝色絮状沉淀,并出现黑色固体 |
小科咨询老师后得知蓝绿色沉淀为碱式铜盐。
实验结论:
实验反思:实验中生成氢氧化铜沉淀的原理是。
方案一:把钠块和无水硫酸铜直接混合,在干燥的空气中加热。
方案二:把钠块和无水硫酸铜直接混合,隔绝空气加热。
从两个方案中,选择出更合理的方案并给出理由。

资料:①膨松剂在面包制作过程中发生反应:2NaHCO3 Na2CO3+H2O+CO2↑,
NH4HCO3 NH3↑+ H2O + CO2↑;
②氨气溶于水所得溶液为氨水,呈碱性。
实验操作:
第1步:关闭K2 , 打开K1 , 经过加热,D中酚酞变红。
第2步:关闭K1 , 打开K2 , 加热至试管B中的水里气泡不再产生。
第3步:观察到大试管中还有剩余物质。
根据以上信息回答以下问题:
请回答下列问题:

实验设计:三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注射器,C颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。
实验操作:
NaCl+NH3+CO2+H2O==NH4Cl+NaHCO3↓
过滤出碳酸氢钠晶体,再受热分解得到产品:2NaHCO3 Na2CO3+H2O+CO2↑

试回答下列问题:

