| 选项 | 归类 | 物质(或仪器、变化) |
| A | 缓慢氧化 | 金属生锈、食物变质、光合作用 |
| B | 可燃性气体 | 氢气、氧气、一氧化碳 |
| C | 大气污染物 | SO2、CO、CO2 |
| D | 可直接加热的仪器 | 试管、蒸发皿、燃烧匙 |
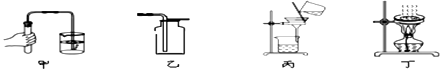
| 选项 | 需区分的物质 | 方法一 | 方法二 | |
| A | 氮气和二氧化碳 | 使用燃着的木条 | 通入紫色石蕊试液 | |
| B | 硬水和软水 | 加入肥皂水,振荡 | 加入明矾,振荡 | |
| C | 过氧化氢溶液和水 | 加二氧化锰 | 观察颜色 | |
| D | 食盐和碳酸钙 | 滴加稀盐酸 | 加水 | |
| 序号 | 化学反应事实 | 影响化学反应的因素 |
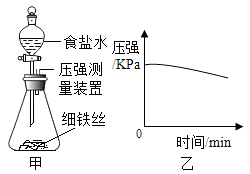
| A | 细铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
| B | 碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 | 反应温度 |
| C | 某双氧水常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂 |
| D | 与相同浓度盐酸反应,粉末状石灰石比块状石灰石反应快 | 反应物的种类 |
A 干冰 B 明矾 C 氧气 D 酒精 E 石墨 F 氦气

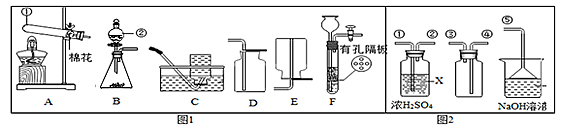
(查阅资料)废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。
(实验1)废干电池的拆卸与处理
①兴趣小组同学将废旧干电池卸下的锌筒、碳棒冲洗干净,备用。
②将铜帽放入盐酸中,除去锈污,冲洗备用。
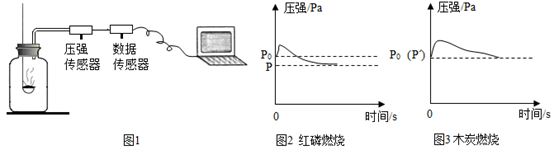
(实验2)检验废干电池筒内黑色固体中MnO2的存在
兴趣小组同学设计了如下图所示的实验:

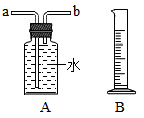
用锌皮和稀硫酸制取氢气。用适当的发生装置,采用排水法收集并测定氢气的体积(如图),气体从装置A导管口(填“a”或“b”)进。
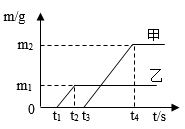
①把干燥纯净的24.5g氯酸钾和5.5g二氧化锰混匀、装入大试管中,加热。
②待反应完全后,将试管冷却、称量,得到20.4g残留固体。
③再将残留固体经溶解、过滤、洗涤、干燥、称量,得到5.5g黑色固体。
[数据分析]
①该实验说明:二氧化锰在氯酸钾分解反应前后,不变。
②完全反应后制得氧气的质量是g。(提示:已知所有化学反应遵循如下规律:参加化学反应的各物质的质量总和等于反应后各生成物的质量总和)
[实验反思]
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较的大小。该实验说明:二氧化锰在氯酸钾分解反应前后,不变。

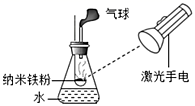
(提出问题)淡黄色固体是什么?
①硫粉是一种淡黄色固体,难溶于水,燃烧生成刺激性气味的有毒气体。
②过氧化钠(Na2O2)是一种淡黄色固体,能与水反应放出气体。
(猜想与探究)猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.。
方案一:取少量该固体粉末于试管中,加5mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
经过讨论,兴趣小组决定采用方案一,其理由是(选填字母,可多选)
A 操作简单B 无实验污染C 节约能源

①若无现象,则此粉末为,
②若淡黄色粉末为过氧化钠,可观察到试管中的现象是,烧杯中出现气泡,说明。
(实验结论)实验确定该淡黄色粉末是过氧化钠。
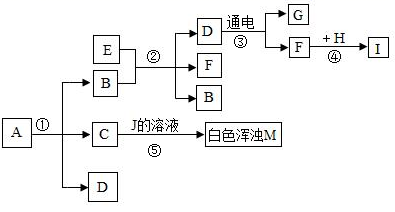
反应②的化学式表达式为:。
反应③的化学式表达式为:。
反应⑤的化学式表达式为:。
a.电能转化为化学能 b.化学能转化为电能