| 物质 | 食醋 | 酱油 | 食盐水 | 牙膏 | 肥皂 |
| pH | 2~3 | 4~5 | 7 | 8~9 | 9~10 |
夏天我们被蚊虫叮咬后,蚊虫会在人的皮肤内分泌蚁酸(一种酸),从而使皮肤肿痛。要减轻痛痒,可在叮咬处涂抹下列物质中的( )
 B .
B . 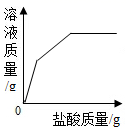 C .
C . 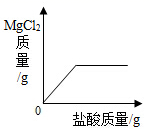 D .
D . 
①所配稀盐酸中溶质的质量为g,所需浓盐酸的质量为g。
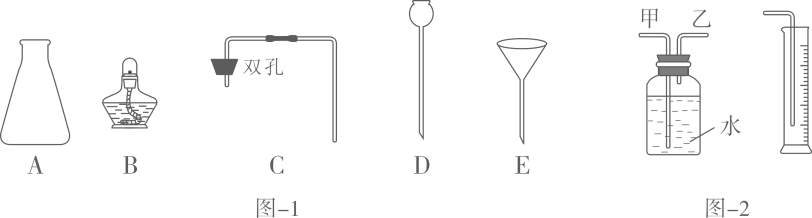
②已知浓盐酸密度为1.19g/cm3 , 量取上述所需浓盐酸用到的仪器是(填标号)。
A、10mL量筒
B、50mL量筒
C、试管
D、胶头滴管
③测定所配稀盐酸的酸碱度,应将pH试纸放置在上。
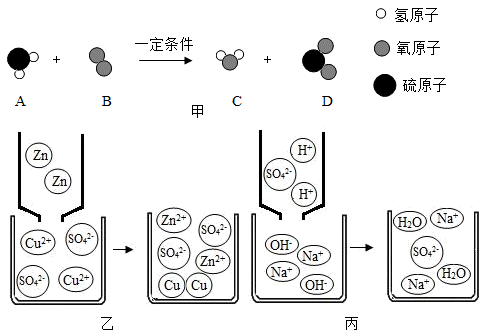
①铁与稀盐酸反应的化学方程式为。
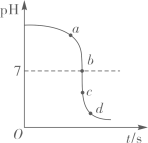
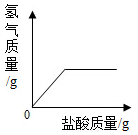
②下列示意图中,与实验结果相符的是(填标号)。

A、BaCl2溶液
B、酚酞溶液
C、石蕊溶液
D、Na2CO3溶液
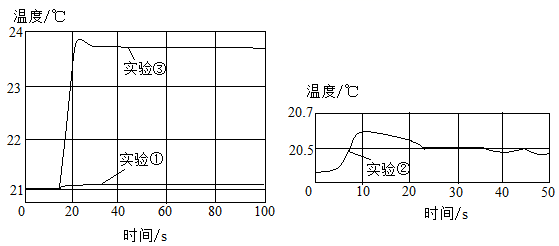
①50mL一定浓度的盐酸与50mL蒸馏水混合,测量溶液温度的变化。
②50mL一定浓度的氢氧化钠溶液与50mL蒸馏水混合,测量溶液温度的变化。
③50mL一定浓度的盐酸与50mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
用数字化实验技术测得3个实验,溶液温度随时间变化的关系如图所示。
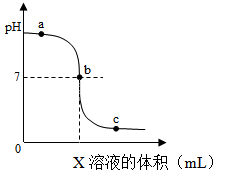
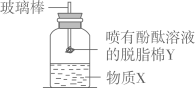
在50mL一定浓度的氢氧化钠溶液中滴加2~3滴酚酞试液,再逐滴加入一定浓度的盐酸,并用玻璃棒搅拌,溶液颜色由红色刚好变为无色时,可说明两者发生了反应。该反应的化学方程式为。
查阅资料:酚酞在pH<8.2的溶液中呈无色,在8.2<pH<14的溶液中呈红色。
作出猜想:猜想一:NaCl
猜想二:NaCl、NaOH
猜想三:NaCl、NaOH和Na2CO3
同学们讨论后一致认为猜想是错误的,理由是。
实验验证:取样,滴加,无气泡产生,猜想三不正确。
原因分析:反应后无色溶液中仍存在少量NaOH,加热蒸发,当溶液的pH在范围内,溶液的颜色变红。
总结反思:向某碱性溶液中滴加2~3滴无色酚酞试液,振荡后溶液的颜色(填“一定”或“不一定”)变红。
|
实验编号 |
硫酸的质量分数/% |
硫酸的体积/mL |
锌粒的质量/g |
时间/s |
|
1 |
10 |
10 |
1 |
78 |
|
2 |
10 |
10 |
2 |
57 |
|
3 |
40 |
10 |
1 |
9 |
①比较实验1、2的数据,可以得出的结论是。
②由实验数据可知,该实验中对Zn与稀硫酸反应快慢影响较大的因素是。
③比较不同条件下锌粒与稀硫酸反应的快慢有不同的方法,除测量产生相同体积的H2所需的时间,还可采用的测量方法是(写出一种)。
已知:①BaSO4+4C 4CO↑+BaS,②CaO、BaO都能与水反应生成碱


a.NaOH溶液 b.生石灰 c.Ba(OH)2溶液 d.BaO固体
证明铁已除尽的方法是:取少量上层清液于试管中,滴入足量溶液,若观察到,则已除尽。