| 选项 | 事实 | 解释 |
| A | 酒精溶液不能导电 | 溶液中没有自由移动的带电粒子 |
| B | 稀硫酸、稀盐酸都能使紫色石蕊溶液变红色 | 溶液中都含有氢离子 |
| C | 白色纸张沾浓硫酸后变黑 | 浓硫酸具有吸水性,能使纸张炭化 |
| D | 硫酸铜和氯化铜溶液都呈蓝色 | 溶液中都含有铜离子 |
 蒸发食盐水
B .
蒸发食盐水
B . 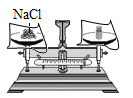 称取一定量氯化钠固体
C .
称取一定量氯化钠固体
C . 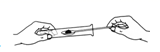 向试管中加入食盐粉末
D .
向试管中加入食盐粉末
D . 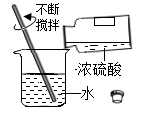 稀释浓硫酸
稀释浓硫酸

步骤1:从A处通入空气,点燃酒精灯,观察到硫粉熔化、燃烧,产生微弱的淡蓝色火焰;
步骤2:从A处改通入氧气,观察到硫燃烧产生明亮的蓝紫色火焰。
下列说法错误的是( )
| 选项 | X的物质类别 | 观点描述 |
| A | 金属 | 若X为Cu,则反应能够发生 |
| B | 金属氧化物 | 若X为MgO,则Y为H2O |
| C | 碱 | 若X为NaOH,则盐为Na2SO4 |
| D | 盐 | 若X为BaCl2 , 则生成白色沉淀 |
 D . 稀盐酸溶液
D . 稀盐酸溶液 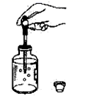 B . 熄灭酒精灯
B . 熄灭酒精灯  C . 蒸发食盐水
C . 蒸发食盐水  D . 稀释浓硫酸
D . 稀释浓硫酸 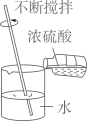
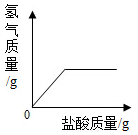 B .
B . 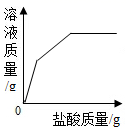 C .
C . 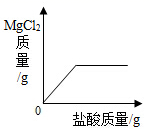 D .
D . 
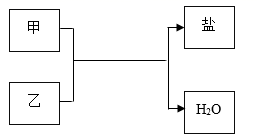
| 选项 | 甲 | 乙 |
| A | Fe2O3 | 稀硫酸 |
| B | SO3 | NaOH溶液 |
| C | 稀盐酸 | Ca(OH)2溶液 |
| D | 稀盐酸 | AgNO3溶液 |
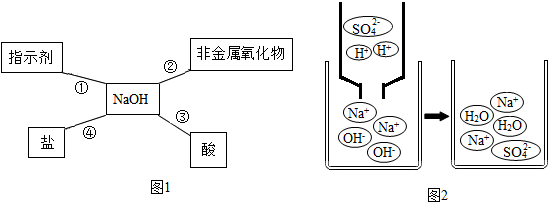
①和镁条的反应:。
②和碳酸钠溶液反应:。
③和氯化钡溶液反应:。
上述反应中属于复分解反应的有;属于酸的共同性质的有 (填编号);不同的酸性质差异的原因。
①金属表面除锈 ②制造药物氯化锌 ③除去氯化钠中的少量碳酸钠

A小组同学发现实验台上摆放的药品中(如图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
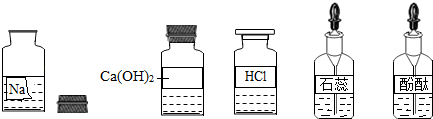
(提出问题)这瓶溶液是什么溶液?
(获得信息)
酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
(提出猜想)这瓶溶液可能是:1、氯化钠溶液;2、氢氧化钠溶液;3、碳酸钠溶液。
(实验推断)
(继续探究)另取样品加入过量的CaCl2溶液,可观察到有产生,反应的化学方程式为,设计这一步骤的目的是;静置后,取上层清液,滴入酚酞试液,溶液呈红色。
(探究启示)实验取完药品后应。
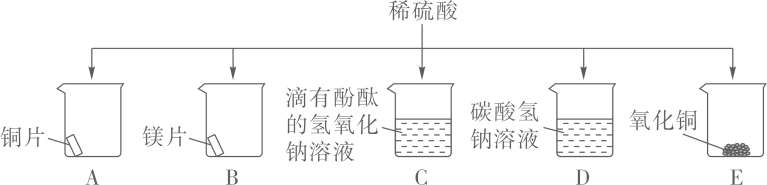
(提出问题)铜与硫酸真的不能反应吗?
(查阅资料)
①铜与浓硫酸反应的化学方程式:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O
②SO2能使品红溶液褪色;
③SO2能与碱溶液反应;
④SO2能溶于水,但不溶于饱和NaHSO3溶液
(进行实验)
同学们在老师的帮助下用如图所示装置进行实验:

请回答下列问题:
实验开始时,打开开关K,发现D中品红溶液褪色,装置D中试管口放置的棉花上浸有浓氢氧化钠溶液,其作用是。
A、水
B、氢氧化钠溶液
C、饱和石灰水
D、饱和NaHSO3溶液
(知识拓展)化学反应的进行与物质的溶质质量分数,反应条件都有一定的关系。
|
实验编号 |
① |
② |
③ |
④ |
⑤ |
|
稀硫酸的质量(g) |
20.0 |
40.0 |
60.0 |
80.0 |
100.0 |
|
溶液的总质量(g) |
120.0 |
140.0 |
159.78 |
179.56 |
199.56 |
请回答下列问题:
