 B .
B .  C .
C .  D .
D . 
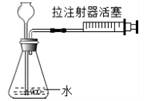 B . 检验氧气是否收集满
B . 检验氧气是否收集满  C . 稀释浓硫酸
C . 稀释浓硫酸  D . 测定溶液的酸碱性
D . 测定溶液的酸碱性 

| 选项 | 物质(括号内为杂质) | 除杂方法 |
| A | 二氧化锰(高锰酸钾) | 加热固体混合物 |
| B | 氮气(氧气) | 将气体缓缓通过足量的灼热铜网 |
| C | 二氧化碳(一氧化碳) | 将气体通入足量的氢氧化钠溶液,干燥 |
| D | 氯化钠(碳酸钠) | 将固体溶解在水中,滴加适量的氢氧化钙溶液,过滤后蒸发结晶 |



①将甲溶液分别与其他三种溶液混合,都有白色沉淀生成;
②将乙溶液与丁溶液混合,有气泡产生;
③向丙溶液中滴入AgNO3溶液,出现白色沉淀,加稀硝酸后,沉淀不消失;
分析实验得到的以下结论中错误的是( )
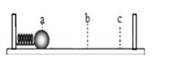



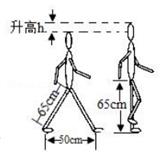
请回答下列问题:

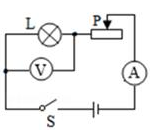
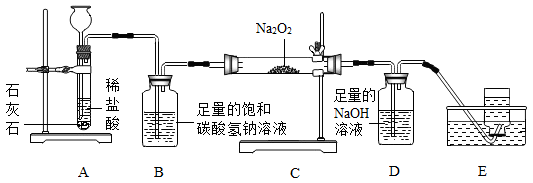
【猜想与假设】猜想一:Na2CO3猜想二:Na2CO3和Na2O2
猜想三:Na2CO3和NaOH猜想四:
|
操作 |
现象 |
结论 |
|
① 取少量样品于试管中,加入足量的水,振荡 |
固体完全溶解,且 |
样品中一定没有 Na2O2 |
|
② 取少量实验①所得溶液于另一试管中,加入过量的 BaCl2溶液振荡 |
有白色沉淀产生 |
猜想三正确 |
|
③ 取少量实验②所得的上层清液于另一试管中,加入过量的溶液,振荡。 |
有蓝色沉淀产生 |

【查阅资料】
① Fe3+ 可与硫氰化钾 溶液反应,从而溶液会显红色,且Fe3+的浓度越大,溶液红色越深;而Fe2+遇硫氰化钾 溶液不会显红色。
② 高锰酸钾(KMnO4)溶液可以与盐酸反应,而不与稀硫酸反应。
③ 稀硝酸可以将 Fe2+氧化成Fe3+ 。
Ⅰ.小科进行了以下实验,来检测该补铁药品中是否含有Fe3+并探究维生素C的作用:

本实验中的试剂2与实验Ⅰ中的试剂1都可以是 (填序号)。



|
实验次数 |
1 |
2 |
3 |
4 |
|
加入稀硫酸质量/克 |
20 |
20 |
20 |
20 |
|
剩余固体质量/克 |
20.0 |
17.4 |
14.8 |
13.5 |
请分析计算:

|
型号 |
额定电压 |
额定电流 |
堵转电流 |
|
RS﹣360SH﹣14280 |
12V |
0.3A |
1.5A |
请根据以上信息计算: