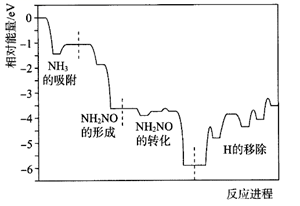

反应原理:
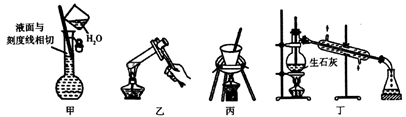
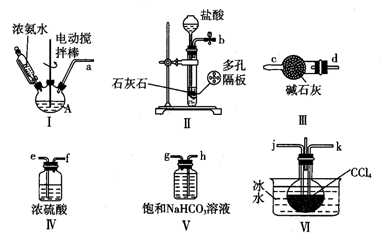
实验室可选用下列装置制备氨基甲酸铵 。
回答下列问题:
A.蒸馏 B.高压加热烘干 C.真空微热烘干
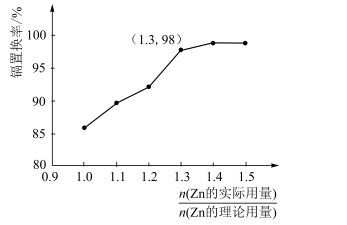
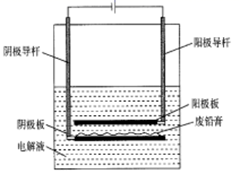
①实际生产中 比值最佳为1.3,不宜超过该比值的原因是。
②若需置换出112kgCd,且使镉置换率达到98%,实际加入的Zn应为kg。
i. COS(g)+H2(g) H2S(g)+CO(g)△H1=-17kJ/mol
ii. COS(g)+4H2(g) H2S(g)+CH4(g)+H2O(g) △H2
已知:CH4(g)+H2O(g) CO(g)+3H2(g)△H=+206kJ/mol,则△H2=。
①0-5min内,v(COS)=。
②反应i的平衡常数K=。
③若在起始温度为T1℃的绝热容器中重复上述实验,H2的平衡分压P2P1(填“>”“=”或“<”),理由为。

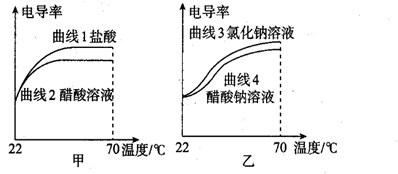
由图可知,增大NaOH溶液的初始浓度,COS的吸收速率(填“增大”“减小”或“不变”),判断依据为。
|
GaN |
GaP |
GaAs |
|
|
熔点 |
1700℃ |
1480℃ |
1238℃ |

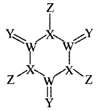
①晶胞中镓原子采用六方最密堆积,每个镓原子周围距离最近的镓原子数目为。
②从GaN晶体中“分割”出的平行六面体如图乙。若该平行六面体的高为 ,GaN晶体的密度为
(用
表示)。
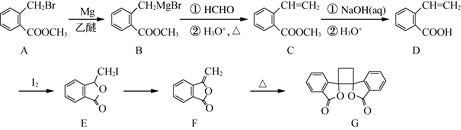
①能发生银镜反应;
②碱性水解后酸化,其中一种产物能与FeCl3溶液发生显色反应;
③分子中有4种不同化学环境的氢。