
 白磷始终不燃烧
B .
白磷始终不燃烧
B .  小气球变瘪
C .
小气球变瘪
C .  U型管内液面左高右低
D .
U型管内液面左高右低
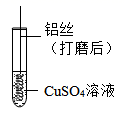
D .  验证Fe、Cu、Ag的金属活动性强弱
验证Fe、Cu、Ag的金属活动性强弱



a 熟石灰 b 氢氧化钠 c 氯化钠
a 金属材料 b 合成材料 c 复合材料
a 白醋 b 食盐水 c 纯碱溶液
a 烧纸 b 刺激性 c 烧焦羽毛
煮馄饨用水是硬水还是软水,可以用检验。
煮馄饨用燃料是天然气,天然气的主要成分(写化学式)。

可选用的装置组合为;若改用高锰酸钾制氧气,需对装置做出的改动为。

①打开止水夹1及分液漏斗活塞,待液体充满大试管后,关闭止水夹1及分液漏斗活塞.观察到液体分层,钠熔成银白色小球,产生大量气泡,下层溶液变成红色,并逐渐被压入B中;
②打开止水夹2,待B中部分溶液进入C中,迅速关闭止水夹2,A中反应的化学方程式为;
③打开止水夹3,稀盐酸进入C中,并观察到(填实验现象),说明二氧化碳能与氢氧化钠溶液反应且进入的稀盐酸过量;
④将燃着的木条伸到导管尖嘴处,打开止水夹1,气体燃烧,产生色火焰。
查阅资料:
Ⅰ:硫酸亚铁铵,俗称摩尔盐,是一种重要的化工原料。易溶于水,不溶于酒精,在100-110℃时分解,110℃完全失去结晶水。温度升高,(NH4)2Fe(SO4)2会继续分解。
Ⅱ:硫酸亚铁,容易被氧气缓慢氧化,铁粉能防止溶液中的硫酸亚铁被氧化,能与硫酸铵反应生成硫酸亚铁铵。
Ⅲ:铁屑中硫化物与稀硫酸反应会产生酸性硫化氢(H2S)气体,要净化处理。
小组同学设计了如下图1流程制备硫酸亚铁铵晶体:

根据流程回答下列问题:
步骤①中用热碱性溶液浸泡废铁屑目的是除去铁屑上面的油污,可以选择的浸泡液是。
A 碳酸钠溶液 B 氯化钠溶液 C 稀盐酸

根据装置图回答下列问题:
B装置中产生大量氢气作用:一是可以将装置及溶液中氧气排走,防止硫酸亚铁被氧化,该操作是;二是通过关闭活塞b、c,打开a,将反应后B中溶液压入A中。
小组同学设计了图3实验装置来测定x值:

实验步骤:
①连接好装置,检查装置气密性,在A中放入一定质量的硫酸亚铁铵
②打开弹簧夹,通入一段时间的N2后,称量B装置质量
③关闭弹簧夹,将恒温加热器控制在110℃进行加热至晶体完全失水: (NH4)2Fe(SO4)2·xH2O=(NH4)2Fe(SO4)2+ xH2O
④打开弹簧夹,继续缓缓通入一段时间的N2 , 再次称量B装置质量,两次称量质量差为10.8g
⑤称量A中反应后固体质量为28.4g
……
根据实验装置图和实验步骤回答下列问题
将加热温度控制在110℃的目的是。
A 步骤2中先称量,再通入一段时间的N2 , 会导致x值偏大
B 步骤3中如果加热时间不够,会导致x值偏小
C 步骤4中缓缓通入一段时间的N2 , 目的是将装置中残留的水蒸气被B装置充分的吸收
D C装置作用是吸收空气中二氧化碳,防止进入B中
