 B . 风力发电
B . 风力发电  C . 太阳能供热
C . 太阳能供热  D . 蓄电池放电
D . 蓄电池放电 



| 实验操作 | 甲+乙 | 乙+丙 | 甲+丙 |
| 实验现象 | 有气泡冒出 | 有白色沉淀 | 无明显现象 |
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | NaCl固体 | 泥沙 | 加足量水溶解,过滤 |
| B | FeSO4溶液 | CuSO4溶液 | 加入过量铁粉,过滤 |
| C | H2 | HCl | 通过足量氢氧化钠溶液,干燥 |
| D | 稀盐酸 | 稀硫酸 | 加入适量氯化钡溶液,过滤 |

①可作燃料的气体
②一种难溶性的碱
③可作干燥剂的酸
④常作调味品的盐
①以下食物中富含蛋白质的是(填序号)

②下列餐厅用品所使用的主要材料,属于有机高分子材料的是(填序号)

③黄瓜中富含维生素C,维生素C的化学式为C2H8O6 , 在维生素C中碳、氧两种元素的原子个数之比为(填最简整数比)。维生素C在 pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在烹饪时应加入少量的(填序号)。
A小苏打 B食盐 C食醋
④餐厅里烧水的锅炉用久后内壁会出现水垢,水垢的主要成分是碳酸钙,在碳酸钙中,所含元素质量分数最大的是(填元素符号)。
⑤餐厅里切菜的铁质菜刀,用完后擦洗不净常会生锈,铁生锈是铁与空气中的(填物质名称)等物质发生化学反应的结果。

请用化学方程式表示过程②中发生的化学反应∶
在上述①一④的生产过程中,没有涉及到的化学反应类型是反应。(填“化合”“置换” “分解”“复分解”之一)

①由图一可知,20℃ 时,100g 水中加入40gNaCl固体充分溶解,所得溶液的质量为g。②由图一可知,50℃ 时,KNO3溶液的溶质质量分数NaCl溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
③如图三所示,20℃ 时,将盛有饱和石灰水的小试管放入盛水的烧杯l中,向水中加入氢氧化钠固体,结合图二分析石灰水中可出现的现象。
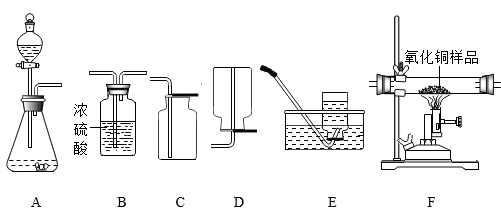
①所选仪器的连接顺序为(填写仪器序号字母)。
②生成氧气时,所发生反应的化学方程式为∶
③反应结束后,进行过滤操作可回收二氧化锰,过滤时用到的玻璃仪器除烧杯和玻璃棒外,还需要。
(已知∶ CuO+H2 Cu+H2O,其中 B1、B2、B3为三个浓硫酸洗气瓶)。
①小娟同学欲通过测量反应前后B2浓硫酸洗气瓶的质量变化,测算氧化铜样品中CuO的质量分数。实验中,在其他操作正常的条件下,若装置中不连接 B1 , 则测算结果将(填“偏小”“偏大” “不受影响”之一)。
②若所有的操作正常,测得B2洗气瓶的质量增加ag,则F处大玻璃管内的物质总质量应该减少g(计算结果可为分数形式)。

①纯碱的名称是,其水溶液能使无色酚酞试液变
②下列有关过程③中能量转化的说法,正确的是(填选项序号)。
A化学能转化为电能 B电能转化为化学能 C潮汐能转化为化学能
①A点处的溶质是(填化学式)。
②求恰好完全反应时,所得不饱和溶液的质量。


试根据实验过程和现象做出判断并回答∶