
| 操作 | 实验现象 | 推断或解释 | |
| A | 将少量饱和硼酸溶液滴加到碳酸钠溶液中 | 无气泡 | 酸性:H2CO3>H3BO3 |
| B | 将C2H4通入溴的四氯化碳溶液中 | 溴的四氯化碳溶液褪色 | C2H4与溴发生了加成反应 |
| C | 同温同压下用pH试纸测定相同浓度的碳酸钠和乙酸铵溶液的酸碱性 | 碳酸钠溶液显碱性,乙酸铵溶液显中性 | 碳酸钠溶液发生了水解,乙酸铵溶液没有水解 |
| D | 向均盛有2mL5%H2O2溶液的两支试管中分别滴入0.3mol/LFeCl3和0.2mol/LCuCl2溶液各1mL | 前者生成气泡的速率更快 | 催化效果:Fe3+>Cu2+ |



|
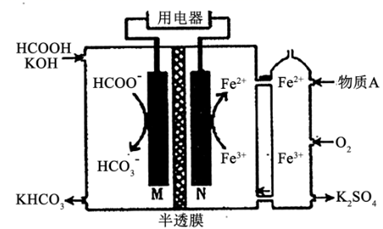
装置I |
装置II |
||
|
烧瓶中 |
分液漏斗中 |
||
|
制备纯净Cl2 |
MnO2 |
浓盐酸 |
|
|
制备纯净NO |
Cu |
稀硝酸 |
水 |
①装置连接顺序为a→(按气流自左向右方向,用小写字母表示)。
②装置IV、V除可进一步干燥NO、Cl2外,另一个作用是。

①样品的纯度为%(保留三位有效数字)
②若在滴定终点时测得溶液中CrO 的浓度是5.0×10-3mol/L,此时溶液中Cl-浓度是。
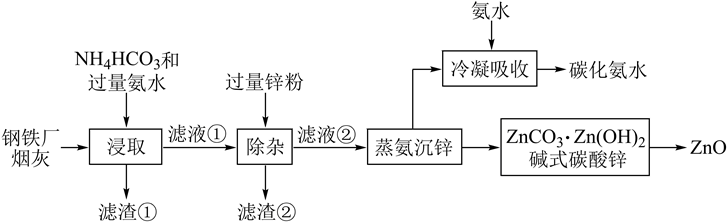 回答下列问题:
回答下列问题:

请回答下列问题:
①写出反应II的热化学方程式。
②反应I和反应II中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g) 2NO2(g)反应速率的是(填“反应I”或“反应II”),请写出判断的理由。
| 浓度(mol·L-1) 时间(min) | NO | CO2 | N2 |
| 0 | 0.200 | 0 | 0 |
| 12 | 0.050 | 0.075 | 0.075 |
| 15 | 0.100 | 0.050 | 0.450 |
①T℃时,该反应的平衡常数为。
②在12min时,若只改变某一条件使平衡发生移动,15min时重新达到平衡,则改变的条件是。
③在15min时,保持温度和容器体积不变再充入NO和N2 , 使NO、N2的浓度分别增加至原来的2倍4倍,此时反应v正v逆(填“>”、“<”或“=”)。

②As4S4俗称雄黄,其中基态As原子的核外电子排布式为[Ar],有个未成对电子。
②研究发现固态PCl5和PBr5均为离子晶体,但其结构分别为[PCl4]+[PCl6]-和[PBr4]+Br- , 分析PCl5和PBr5结构存在差异的原因是。

①锑酸亚铁的化学式为。
②晶体的密度为g·cm-3(设NA为阿伏加德罗常数的值)。
①分子中含有苯环,且能与饱和碳酸氢钠溶液反应放出CO2
②有4种不同化学环境的氢,且原子个数比为6:2:1:1
③苯环上的一元代物只有一种结构
 的路线流程图(无机试剂任用,流程图形式见题干)。
的路线流程图(无机试剂任用,流程图形式见题干)。