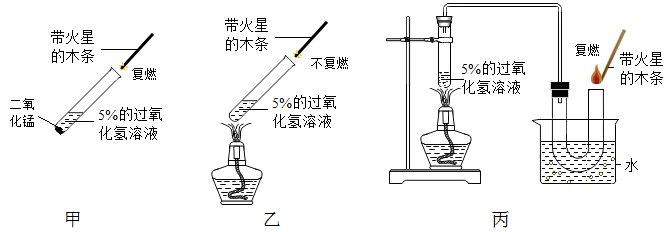
B . 收集氧气
B . 收集氧气  C . 验满
C . 验满 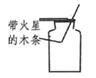 D . 性质检验
D . 性质检验 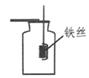
 B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 

| A | B | C | D |
| | | | |
| 集气瓶中灌 水 | 集气瓶中灌 | 导管伸入到集气瓶体积的 | 导管伸入到集气瓶体积的 |

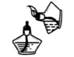 C . 加热高锰酸钾
C . 加热高锰酸钾  D . 收集氧气
D . 收集氧气  B .
B .  C .
C .  D .
D . 

 B . 收集
B . 收集  C .
C .  验满
D . 验证性质
验满
D . 验证性质 


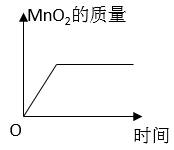 B .
B . 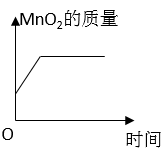 C .
C .  D .
D . 

a.将烧杯换成液面高度相同水槽
b.导管伸入水中位置过深,气体无法逸出
c.先用手捂住试管壁,再将导管另一端插入水中
c.可能是塞子未塞紧
|
1 |
空气 |
NH3 |
CH4 |
HCl |
O2 |
|
密度/g•L-1 |
1.293 |
0.771 |
0.717 |
1.629 |
1.43 |
|
溶解性 |
—— |
极易溶 |
难溶 |
极易溶 |
难溶 |



①当气泡连续均匀地冒出时,将导管伸入集气瓶口
②将装满水的集气瓶倒置在水槽中
③当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面放置
④熄灭酒精灯
⑤导管移出水面





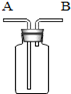
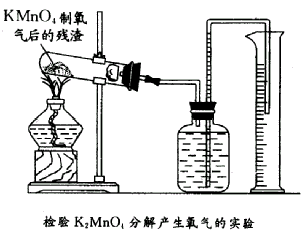
换算成标准状况下的体积为248 mL,而实际测得的氧气为308 mL(标准状况),超过理论量为:(308一248)mL=60mL。试回答:
①它是由氢气和氧气组成的 ②它是由氢元素和氧元素组成的
③它是由一个氢分子和一个氧分子构成的 ④它由两个氢元素和两个氧元素组成
(填写图中的数字序号)。



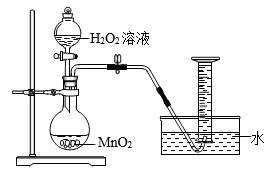
【提出问题】水是如何减缓该反应速度的呢?
【建立假设】水可以降低H2O2溶液浓度,从而减缓反应速度
【实验方案】他利用如图装置,在相同条件下,分别用30毫升的1%、3%和7%的H2O2溶液进行实验, 观察并比较。
【实验结论】加水降低了H2O2溶液的浓度, 使反应速度变慢。
【交流反思】

| 实验1 | 实验2 | 实验3 | |
| 2%的H2O2溶液体积/毫升 | 20 | 20 | 20 |
| 温度/摄氏度 | 20 | 80 | 20 |
| 相同时间集气瓶内气体体积 | 较多 | 最多 | 最少 |
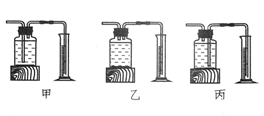
| 双氧水的质量 | 双氧水的浓度 | ? | |
| Ⅰ | 50.0g | 1% | |
| Ⅱ | 50.0g | 2% | |
| Ⅲ | 50.0g | 4% |