编号 | 事实 | 结论 |
A | 某气体不能使带火星木条复燃 | 该气体一定不含氧气 |
B | 某物质可以导电 | 该物质一定是金属单质 |
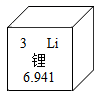
C | 某元素原子的质子数为6 | 该原子核外电子数也一定为6 |
D | 某物质完全燃烧,生成物只有CO2和H2O | 该物质一定由C、H、O三种元素组成 |
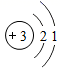

|
物质 |
H2 |
N2 |
NH3 |
|
沸点/℃(1.01×105 Pa) |
–252 |
–195.8 |
–33.35 |
在1.01×105 Pa时,要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,最适宜的温度应该控制在℃≤ T <℃。

①加入一定量的锌粉后,一定发生的反应的化学方程式为。
②往滤渣中加盐酸,发现有气泡产生,则反应后滤渣中一定有的是,滤液中一定含有的溶质是,一定不含有的溶质是。

(实验方案)如图所示
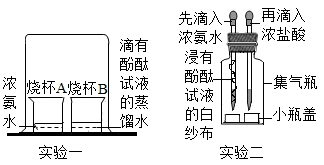
(实验现象)
实验一中的现象是。
微观上,说明微粒具有的性质是。宏观上,从物质的性质或变化的角度分析,你得出的结论是(写一点)。
实验二避免了实验一的不足,改进后的优点有(写一点)。
(查阅资料)
氨气在加热条件下能与氧化铜反应:2NH3+3CuO 3X+N2+3H2O,X的化学式是。

(数据处理与误差分析)
充分反应后,测得A、B、C三个装置在反应前后的质量变化如下表所示
|
装置 |
A |
B |
C |
|
数据 |
减少了4.8g |
增加了6.0g |
增加了2.8g |
甲同学利用A、B、C三组装置所提供的数据,乙同学利用B、C两组装置所提供的数据,计算出的氮、氢元素的质量比都与理论值明显不符,分析产生误差的原因是。
在一定条件下,可用氮气和氢气制得氨气。工业上常用氨气生产氮肥(NH4)2SO4 , 施肥时,要避免与之混用的是_____(填序号)。