 可回收物
B .
可回收物
B .  厨余垃圾
C .
厨余垃圾
C .  有害垃圾
D .
有害垃圾
D .  其他垃圾
其他垃圾
 B . 量取一定体积的水
B . 量取一定体积的水  C . 将水倒入烧杯
C . 将水倒入烧杯  D . 溶解NaOH固体
D . 溶解NaOH固体 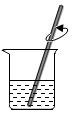


| 选 项 | 事实 | 解释 |
| A | 氧气(O2)和臭氧(O3)性质不同 | 构成物质的分子不同 |
| B | 稀有气体的性质稳定 | 其原子已达到相对稳定结构 |
| C | 变瘪的乒乓球放入热水中能鼓起来 | 分子大小随温度改变而改变 |
| D | 50mL水和50mL酒精混合后的溶液体积小于100mL | 分子间有间隔 |

| 物质 | 甲 | 乙 | 丙 | 丁 |
| t1时的质量/g | 51 | 9 | 3 | 17 |
| t2时的质量/g | 23 | 3 | x | 51 |
 关闭分液漏斗活塞,向右拉动注射器活塞,松手后注射器活塞又弹回
B .
关闭分液漏斗活塞,向右拉动注射器活塞,松手后注射器活塞又弹回
B . 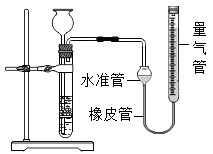 长颈漏斗加水至浸没下端,从量气管加水,水准管内液面低于量气管内液面
C .
长颈漏斗加水至浸没下端,从量气管加水,水准管内液面低于量气管内液面
C . 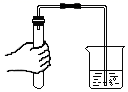 导气管放入水中,导管内液面低于烧杯内液面;或者手握试管,导管口有气泡
D .
导气管放入水中,导管内液面低于烧杯内液面;或者手握试管,导管口有气泡
D .  关闭弹簧夹,从长颈漏斗加水液封下端;继续加水,长颈漏斗内液面与试管液面相平
关闭弹簧夹,从长颈漏斗加水液封下端;继续加水,长颈漏斗内液面与试管液面相平
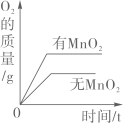 两份完全相同的双氧水在有无MnO2情况下产生O2
B .
两份完全相同的双氧水在有无MnO2情况下产生O2
B .  在密闭容器中用红磷测定空气中氧气的含量
C .
在密闭容器中用红磷测定空气中氧气的含量
C .  向等质量等质量分数的稀硫酸中,分别加入足量的铁粉和锌粉
D .
向等质量等质量分数的稀硫酸中,分别加入足量的铁粉和锌粉
D . 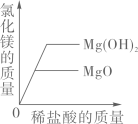 向等质量的氧化镁、氢氧化镁中,分别加入质量分数相同的稀盐酸至过量
向等质量的氧化镁、氢氧化镁中,分别加入质量分数相同的稀盐酸至过量
| 序号 | 物质 | 杂质 | 所用试剂和操作方法 |
| A | NaCl固体 | Na2CO3 | 加入足量水溶解、过滤 |
| B | 铁粉 | Fe2O3 | 加入适量的稀盐酸、过滤 |
| C | H2 | HCl | 通过足量的AgNO3溶液、干燥 |
| D | NaNO3溶液 | Na2S | 加入过量的 |

① 二氧化硫 ② 一氧化碳 ③ 碳酸钙 ④ 活性炭 ⑤ 氧化钙 ⑥ 金刚石


A净化水的时候加入明矾是为了杀菌
B用肥皂水可区分硬水和软水
C硬水经过过滤后就能变为软水
D加入洗涤剂能把油脂溶解到水中,更易洗净碗筷
E地球上的水储量是丰富的,但可利用的淡水资源是有限的
F蒸馏水属于纯净物
G长期饮用蒸馏水不利于健康
Ⅰ 若滤渣中有镁粉,则滤渣中除镁粉外还含有(写化学式,下同)。
Ⅱ 若滤渣中有铜粉,则滤液中的溶质一定含有,可能含有。
Ⅲ 若滤渣中没有铜粉,则滤液中的溶质一定含有,可能含有。


高炉内还原机理及实现低碳的途径

(查阅资料)碳在高温下能与水蒸气反应,生成两种常见的气体还原剂。
把一定质量的样品溶解后加入过量的CaCl2溶液,反应的化学方程式为。将所得沉淀(填操作)、洗涤、烘干、称量,判断沉淀已洗涤干净的操作是。
把一定量的样品与足量盐酸反应后,用如图所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液最好采用。

采用如图所示装置,把15.1g含钠的质量分数为42.2%的样品和足量的稀盐酸反应,通过称量反应前后盛有碱石灰的干燥管的质量,利用其质量差求算样品的纯度。该实验的操作步骤有:

①取样品装入广口瓶中,打开止水夹,缓慢鼓入空气数分钟
②关闭止水夹,在干燥管内填满碱石灰,质量为100g
③缓慢加入稀盐酸至不再产生气体为止
④打开止水夹缓慢鼓入空气数分钟,再称量干燥管质量为104.4g
Ⅰ 装置组装完成后,进行步骤①前还必要进行的操作为。
Ⅱ 装置B的作用是;若去掉装置A,测定结果(填“偏大”、“偏小”或“不变”)。
Ⅲ 根据上述数据可以计算出样品中Na2CO3的质量分数为(精确到0.1%)。
Ⅳ 若把最后所得溶液蒸发干,能得到氯化钠的质量为(列最后一步算式即可)。

反应时间(s) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶液温度(℃) | 20.5 | 20.6 | 20.7 | 20.8 | 20.9 | 20.8 | 20.7 |