 B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
| 选项 | A | B | C | D |
| 类别 | 酸 | 碱 | 盐 | 氧化物 |
| 实例 | 硝酸、盐酸 | 熟石灰、烧碱 | 食盐、纯碱 | 水、高锰酸钾 |

③SiO2+2C Si+2CO↑; ④ Si+2NaOH+H2O
Na2SO3+2H2↑。
A.  B.
B.  C.
C.  D.
D.  E.
E. 


请回答下列问题:


他们的结论:铁生锈是因为铁与等发生了化学反应。



【查阅资料】①糯米中加入食用碱可起到中和微生物生成的酸、软化食物纤维等作用;
②草木灰中富含钾盐,主要成分是K2CO3 , 还含有少量K2SO4和KCl。
【实验探究】检验草木灰的成分,并测定草木灰中K2CO3的质量分数。
A.NaOH溶液 B.浓H2SO4 C.NaHCO3饱和溶液 D.酸化的硝酸银溶液
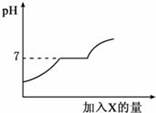
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量。
数据如下表:
|
锥形瓶 |
锥形瓶+稀盐酸 |
锥形瓶+反应后溶液 |
|
|
质量(克) |
35.5 |
55.5 |
80.5 |
每年5、6月是蓝莓丰收的时节,蓝莓中含有丰富的花青素(化学式为C15H11O6)。花青素是一种水溶性色素,颜色与细胞液的酸碱性有关,细胞液酸性时呈红色,碱性时呈蓝色。

|
第1次 |
第2次 |
第3次 |
第4次 |
|
|
加入稀硫酸质量(g) |
100 |
100 |
100 |
100 |
|
剩余固体质量(g) |
87 |
74 |
67.5 |
67.5 |
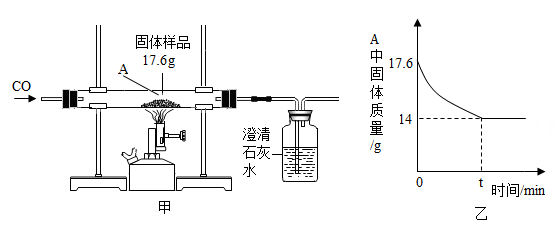
A.节约金属资源 B.加大矿物开采 C.保护环境
