 B . 测溶液的pH值
B . 测溶液的pH值  C . 稀释浓硫酸
C . 稀释浓硫酸  D . 氢气还原氧化铜
D . 氢气还原氧化铜 
 B . 肝脏,分泌的胆汁中含消化酶,对脂肪有乳化作用
B . 肝脏,分泌的胆汁中含消化酶,对脂肪有乳化作用  C . 胰腺,分泌的胰液中含多种消化酶,流入十二指肠帮助消化
C . 胰腺,分泌的胰液中含多种消化酶,流入十二指肠帮助消化  D . 大肠,既能消化又能吸收少量水、无机盐和部分维生素
D . 大肠,既能消化又能吸收少量水、无机盐和部分维生素 
 B . 用船桨划船
B . 用船桨划船  C . 用开瓶器起瓶盖
C . 用开瓶器起瓶盖  D . 用钓鱼竿钓鱼
D . 用钓鱼竿钓鱼 


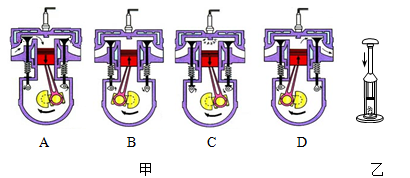
 B .
B . 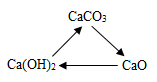 C .
C .  D .
D . 
| 实验目的 | 实验原理 | 主要操作方法 | |
| A | 鉴别稀HCI和稀H2SO4 | 酸根离子的化学性质差异 | 加碳酸钠溶液,观察产生气泡快慢 |
| B | 去除CaCl2溶液中的稀HCl | 不同阳离子的化学性质差异 | 加过量Na2CO3固体、过滤 |
| C | 区别羊毛和棉花纤维 | 不同类别的物质灼烧产生不同的气味 | 取样放于火焰上灼烧,闻气味 |
| D | 除去FeSO4溶液中的少量CuSO4 | 金属活动性差异 | 加过量锌粉,充分反应后过滤 |





胃酸的主要成分 ;草木灰的主要成分 ;具有脱水性;
用于改良酸性土壤 ;天然气的主要成分;用于制造肥皂、造纸 ;



步骤一:取一定量β-淀粉酶,用蒸馏水配成溶液。平分到A、B、C、D试管中,并置于45℃恒温箱待用;
步骤二:在45℃环境中,往A试管加入2mL蒸馏水;B试管加入2mL2%可溶性淀粉溶液;C试管加入2mL含0.1%Ca2+的溶液; D试管加2mL含0.1 %Ca2+的溶液和2%可溶性淀粉溶液;
步骤三:每隔一段时间,测定A、B、C、D四组溶液中β-淀粉酶的活性,分别得到如图所示β-淀粉酶活性的曲线a、b、C、d。则
步骤一:称取3.0g铜粉于容器中,并加入一定质量某浓度的稀H2SO4溶液;
步骤二:再加入3.3克一定浓度的浓硝酸,40℃水浴加热五分钟。
步骤三:调节溶液的pH=4.0,然后过滤、蒸发结晶,并用无水酒精洗涤、干燥制得硫酸铜晶体。
步骤四:改变加入浓硝酸的质量,重复上述实验1-3步操作。测得硫酸铜晶体的质量,计算产率如表。
|
浓硝酸的质量/ g |
3.3 |
4.5 |
5.6 |
6.8 |
8.0 |
9.2 |
10.4 |
11.6 |
12.8 |
14.0 |
15.2 |
|
硫酸铜晶体的产率% |
25.2 |
36.1 |
54.4 |
71.2 |
83.8 |
81.2 |
69.3 |
63.7 |
60.8 |
58.4 |
57.6 |
请回答下列问题:
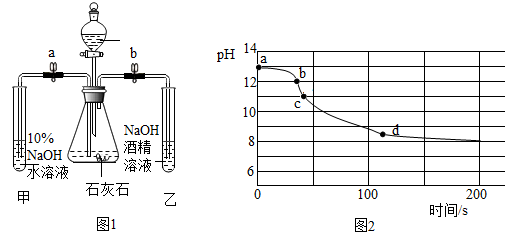
[查阅资料]
①NaOH易溶于酒精,Na2CO3微溶于酒精且都不与酒精反应;
②本实验条件下Na2CO3溶液和NaHCO3溶液的pH最大值可达11.0和8.5,将CO2通入Na2CO3溶液可生成NaHCO3。
[实验探究]打开分液漏斗活塞和止水夹a、b,分别向10%NaOH水溶液和10%NaOH酒精溶液中通入CO2气体。用传感器测得甲试管反应过程中溶液pH值的变化,结果如图2所示。回答:
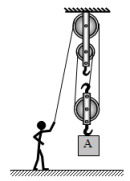
|
实验次数 |
钢球质量(g) |
钢球下摆高度(cm) |
木块滑行距离(cm) |
|
1 |
15 |
22 |
30 |
|
2 |
25 |
22 |
49 |
|
3 |
35 |
22 |
68 |

|
实验序号 |
1 |
2 |
3 |
4 |
|
U(V) |
1.5 |
2.0 |
2.5 |
3.0 |
|
I(A) |
0.25 |
0.28 |
0.31 |
0.34 |




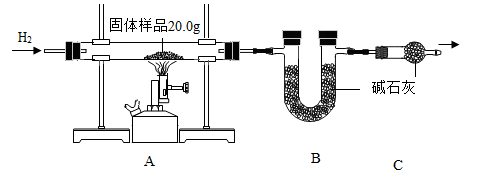
|
物质 |
完全氧化1克所产生的热 |
电压 |
5E |
|
糖类 |
16.8千焦 |
电池容量 |
100mh |
|
蛋白质 |
16.8千焦 |
仪表材料 |
太合金 |
|
脂肪 |
38.9千焦 |
质量 |
54g |
|
打乒乓球第千克体重每小时消耗的能量为18.4千焦 |
最长待机时间 |
5天 |
|
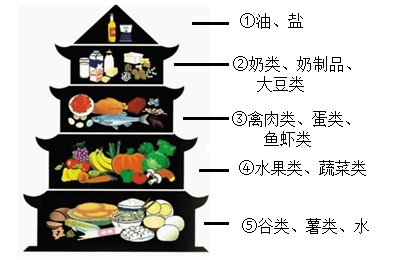
青少年正处在生长发育的关键时期,每天需要补充丰富的以促进细胞生长及组织修复,为此建议适当增加“平衡膳食宝塔”第层食物的摄入(填序号)。