 B . 测定溶液pH
B . 测定溶液pH  C . 倾倒液体
C . 倾倒液体  D . 稀释浓硫酸
D . 稀释浓硫酸 


①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水是由氢元素、氧元素组成,又说明了水分子中氢原子和氧原子的个数之比为2∶1
④既可说明二氧化碳能溶于水,又说明了二氧化碳具有酸性



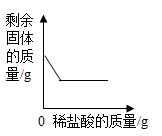 B .
B . 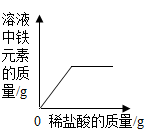 C .
C . 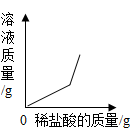 D .
D . 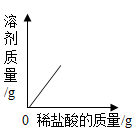

试剂 | 稀盐酸 | 食醋 | 蔗糖水 | 蒸馏水 | 肥皂水 | 烧碱溶液 | 石灰水 |
颜色 | 红 | 红 | 黄 | 黄 | 绿 | 绿 | 绿 |
请分析上表,并回答下列问题:





【查阅资料】Na2CO3溶液的pH>7,与盐酸反应有气泡产生,与Ca(OH)2溶液反应有白色沉淀生成。
【对固体猜想】猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:是NaOH和Na2CO3混合物。
【实验和推断】


碱式碳酸铜和碱式氯化铜分别属于无害锈和有害锈,解释原因:。

①装置丙的作用是。
②实验前、后均需对装置甲、乙、丙进行称重;当装置甲中固体质量不再减少,对装置甲、乙、丙进行再次称重前,需打开活塞再次通入足量的N2 , 其目的是。
③若碱式碳酸铜的化学式为Cu2(OH)2CO3 , 则装置乙将增重克。

①浓硫酸的作用是。
②以下会使Na2CO3质量分数偏大的原因有。
A装置内原有空气中的二氧化碳气体也被碱石灰吸收
B加入稀硫酸的量不足
C反应完成后,装置中仍存有二氧化碳,没有被碱石灰吸收
D装置外的空气中的水蒸气和二氧化碳被碱石灰吸收
方案 | 方案一 | 方案二 |
实验操作 | 在反应后的溶液中滴加氯化钡溶液 | 在反应后的溶液中滴加紫色石蕊试液 |
实验现象 | 出现白色沉淀 | 溶液变红 |
实验结论 | 稀硫酸过量 | 稀硫酸过量 |


|
|
实验一 |
实验二 |
实验三 |
实验四 |
|
食用碱的质量 |
10g |
10g |
10g |
10g |
|
加入CaCl2溶液的质量 |
20g |
40g |
60g |
80g |
|
生成沉淀的质量 |
3g |
m |
8g |
8g |


【提示】①食醋的主要成分是醋酸(HAc),醋酸和碳酸钙反应的化学方程式为:
CaCO3+2HAc=Ca(Ac)2+H2O+CO2↑
②鱼骨中其它成分与食醋反应生成的气体可忽略不计。

